题目内容
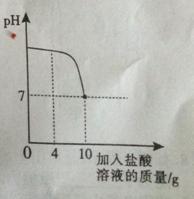
实验室中有一瓶标签被腐蚀的盐酸,小丽为了测定溶液中溶质的质量分数,在烧杯中配制了8克10%的氢氧化钠溶液,然后往烧杯中滴加该盐酸,反应过程中溶液的pH与滴入盐酸的质量关系如图所示。请回答下列问题:
(1)配制8克10%的氢氧化钠溶液,需要水的质量为 g;
(2)计算该盐酸的溶质质量分数;(写出计算过程)
(3)当滴入4克盐酸时,烧杯内溶液中钠元素的质量为 g。
(1)7.2 (2分)
(2)(6分)
解:设盐酸中氯化氢的质量为x。
NaOH + HCl = NaCl + H2O……………(2分)
40 36.5
8g×10% x
40/36.5 = 8g×10%/ x ……………(1分)
x = 36.5 ×0.8g/40 = 0.73g………………………(1分)
盐酸溶液中溶质的 质量分数=0.73g÷10g×100% =7.3%………(1分)
质量分数=0.73g÷10g×100% =7.3%………(1分)
答:盐酸溶液中溶质的质量分数为7.3%。(设、答全对给1分)
(3)0.46………………………………(2分)

同学们在帮助老师整理实验室时,从1、2号橱窗中发现了两瓶失去标签的黑色粉末药品,并确定了这两瓶黑色粉末是木炭粉、铁粉、氧化铜、高锰酸钾中的两种。
他们继续进行了分析、试验和反思:
【查阅资料】 CuO、Fe2O3等金属氧化物与酸反应,生成盐和水
⑴ 分析:小燕同学认为一定不是高锰酸钾,原因是____ _____;
⑵ 实验一:[来源:学科网]
| 实验操作 | [来源:学,科,网Z,X,X,K] | |
| ①取一种黑色粉末少许,加入到稀硫酸中 | 黑色粉末溶解,溶液颜色变__ | 此粉末是氧化铜 |
| ②取另一种黑色粉末少许,加入到稀硫酸中 | 黑色粉末不溶解,没看到气体产生 | 此粉末一 |
⑶ 反思:小华同学认为不做实验①,运用逻辑推理的方法也能得出其中之一是氧化铜的结论,原因是:_______________________________________________________________;
⑷ 实验二:他们又进行了如下实验:将两种黑色粉末混合加热(实验装置如下图),发现黑色粉末逐渐变__ ___,澄清石灰水变____ ___。写出两种黑色粉末发生反应的化学方程式________。
[来源:Zxxk.Com]
 合是
合是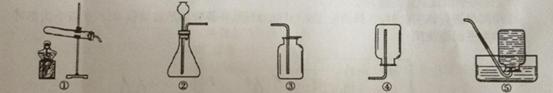
 4X↑+O2↑+2H2O ,其中X的化学式为 ;
4X↑+O2↑+2H2O ,其中X的化学式为 ;

 定不是铁粉
定不是铁粉