题目内容
10.某氯碱工厂排放的尾气里含有有毒的氯气(Cl2),为防止其污染空气,工厂用20%的NaOH溶液吸收氯气(反应的化学方程式为Cl2+2NaOH═NaClO+NaCl+H2O).计算:4吨溶质质量分数为20%的NaOH溶液,理论上可吸收氯气的质量为多少?分析 氯气和氢氧化钠反应生成次氯酸钠、氯化钠和水,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:设理论上可吸收氯气的质量为x,
Cl2+2NaOH═NaCl+NaClO+H2O,
71 80
x 4t×20%
$\frac{71}{x}$=$\frac{80}{4t×20%}$,
x=0.71t,
答:理论上可吸收氯气的质量为0.71t.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.下列实验操作错误的是.
| A. | 木炭放入燃烧匙中加热到发红,然后迅速伸入到氧气瓶底部 | |
| B. | 硫在氧气中燃烧实验所用的燃烧匙内应预先垫上一层石棉布 | |
| C. | 铁丝在氧气中燃烧时,应先将洁净的细铁丝绕成螺旋状 | |
| D. | 细铁丝燃烧的氧气瓶中应先装有少量的水或细沙 |
1.医学上治疗中重度妊娠高血压症需要用到25%的硫酸镁注射液,下表是硫酸镁的部分溶解度数据:
若用无水硫酸镁固体配制10 克25%的硫酸镁溶液,如图为溶液配制过程,
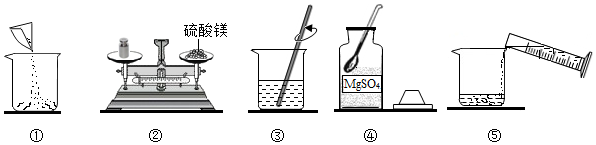
(1)请指出图②中操作错误之处砝码与药品位置放反了
(2)用如图所示的序号表示正确配制该溶液的操作顺序为④②①⑤③
(3)医学人士认为,该注射液在10℃以下不宜使用,请结合上表说明理由:10℃以下时,硫酸镁饱和溶液中溶质质量分数小于25%.
| 温度(℃) | 10 | 20 | 30 | 40 | 60 | 80 |
| 溶解度(g/100g水) | 28.2 | 33.7 | 38.9 | 44.5 | 54.6 | 55.8 |

(1)请指出图②中操作错误之处砝码与药品位置放反了
(2)用如图所示的序号表示正确配制该溶液的操作顺序为④②①⑤③
(3)医学人士认为,该注射液在10℃以下不宜使用,请结合上表说明理由:10℃以下时,硫酸镁饱和溶液中溶质质量分数小于25%.
18.某同学为证明氢氧化钠溶液与盐酸确实进行了反应,设计了一实验:取2ml氢氧化钠溶液入烧杯逐滴滴入盐酸,最后,再滴加酚酞溶液,发现没颜色,说明中和了.
(1)该同学的结论是否正确,原因氢氧化钠显碱性,能使酚酞试液变红色,此时滴加酚酞试液不变色,说明氢氧化钠已被盐酸中和
(2)现只有pH试纸和必要的仪器,设计实验证明该同学的实验酸过量
(2)除pH试纸外,还可选用紫色的石蕊试液、锌粒、碳酸钠等物质做实验出可得同样的结论.
(1)该同学的结论是否正确,原因氢氧化钠显碱性,能使酚酞试液变红色,此时滴加酚酞试液不变色,说明氢氧化钠已被盐酸中和
(2)现只有pH试纸和必要的仪器,设计实验证明该同学的实验酸过量
| 操作 | 现象 | 结论 |
| 将pH试纸放在表面皿上,用玻璃棒蘸取少量反应后的溶液在试纸上,将试纸颜色与标准比色卡对照,读出pH | 溶液的pH<7 | 酸过量 |
20.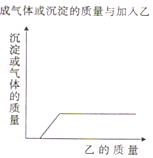 向下表中的甲物质中逐滴加入乙物质溶液至过量,反应生成气体或沉淀的质量与加入乙的质量关系符合如下曲线描述的是( )
向下表中的甲物质中逐滴加入乙物质溶液至过量,反应生成气体或沉淀的质量与加入乙的质量关系符合如下曲线描述的是( )
 向下表中的甲物质中逐滴加入乙物质溶液至过量,反应生成气体或沉淀的质量与加入乙的质量关系符合如下曲线描述的是( )
向下表中的甲物质中逐滴加入乙物质溶液至过量,反应生成气体或沉淀的质量与加入乙的质量关系符合如下曲线描述的是( )| 序号 | 甲 | 乙 |
| A | 碳酸钠和氯化钠的混合溶液 | 硝酸银溶液 |
| B | 稀盐酸和稀硫酸的混合溶液 | 氯化钙溶液 |
| C | 氯化钠和氯化钙的混合溶液 | 碳酸钠溶液 |
| D | 稀盐酸和氯化铜的混合溶液 | 氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
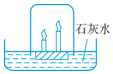 如图,在浮于石灰水上的木块上有一高一矮两支蜡烛,点燃后罩上烧杯,过一会儿,两支蜡烛在没有燃烧完的情况下先后熄灭.则先熄灭的是高(填“高”或“矮”)的蜡烛,此实验还可观察到的现象是石灰水变浑浊,相关的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
如图,在浮于石灰水上的木块上有一高一矮两支蜡烛,点燃后罩上烧杯,过一会儿,两支蜡烛在没有燃烧完的情况下先后熄灭.则先熄灭的是高(填“高”或“矮”)的蜡烛,此实验还可观察到的现象是石灰水变浑浊,相关的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.