��Ŀ����
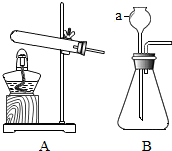
12��������һ����Ҫ�IJ��ϣ���Ӧ��ʮ�ֹ㷺����1�������г����������ˣ���Ҫ������������A������ţ���
A��������B��������C����������
��2������Ʒ����������������ˮ��ͬ���õĽ����д����ֹ����Ʒ�����һ�ַ���������Ʒ����Ϳ�ͻ�ˢ���
��3����ͼ1����һ����AgSO3��Һ�м���ͭ��п�Ļ�Ϸ�ĩ����ַ�Ӧ����ˣ��õ���Һ�����ң�

�������к���п��ͭ�������ֽ���������Һ���������������ӵķ���ΪZn2+����ʱ��������м���ϡ���ᣬ������Ӧ�Ļ�ѧ����ʽΪZn+2HCl�TZnCl2+H2����
������Һ������ɫ������ΪCu+2AgNO3�T2Ag+Cu��NO3��2���û�ѧ����ʽ��ʾ������ʱ��������һ�����е�����������
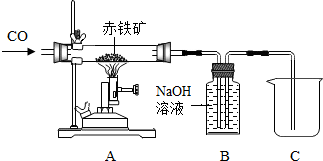
��4��ijС��ͬѧ��һ����̼��ԭ��������ʵ��ⶨij��������������������������ȡ10.0g��������Ʒ����ͼ2װ��ʵ�飬���ʵ����ǰ����Bװ�ã���������ƿ�����ʣ��������ֱ�Ϊ112.3g��118.9g�������ó�������������������������
���� ��1�������������������ù��ܵ��ȿ��ǣ�
��2������������������ͷ�ֹ����Ĵ�ʩ������
��3�������ڽ������˳���У�����ǰ��Ľ�������λ��������Ľ�����������Һ���û��������ɼ��Ϊ��ǰ�ú��ο��ܡ����з�����
��4���ɳ���ʯ��ˮ����118.9-112.3=6.6g�����ݷ�Ӧ��֪����������Ϊ������̼���������������Ļ�ѧ��Ӧ����ʽ����������������������������Ʒ��������������������
��� �⣺��1���������������������ܽ�ú��ȼ�շų����������ݸ��ˣ����������ĵ����ԣ����A��
��2����������������������ˮ��ͬ���õĽ�������������������֪��ֹ������Ĵ�ʩ�У�������Ʒ����Ϳ�ͻ�ˢ����ȣ����������ˮ��������Ʒ����Ϳ�ͻ�ˢ���
��3���ڽ����˳����У������Ļ��˳����п��ͭ��������һ����AgNO3��Һ�м���ͭ��п�Ļ�Ϸ�ĩʱ��п������������Ӧ����п��Ӧ���ͭ������������Ӧ��
�������к���п��ͭ�������ֹ��壬˵������Һ��û��������������ͭ������Һ���������Ľ������ӷ���Ϊ��Zn2+����ʱ��������м���ϡ���ᣬп���뷢����Ӧ����ѧ����ʽΪ��Zn+2HCl�TZnCl2+H2�����÷�Ӧ��һ�ֵ�����һ�ֻ����ﷴӦ��������һ�ֵ��ʺ���һ�ֻ���������û���Ӧ��
������Һ������ɫ��˵����ͭ������������Ӧ����������ͭ����ѧ����ʽΪ��Cu+2AgNO3�T2Ag+Cu��NO3��2����ʱ��������һ�����е�����������
�ʴ�Ϊ����Zn2+��Zn+2HCl�TZnCl2+H2����
��Cu+2AgNO3�T2Ag+Cu��NO3��2������
��4���ⶨʵ�����ݣ�����ʯ��ˮ����6.6g����֪ʯ��ˮ�������������˶�����̼����������������̼������Ϊ6.6g��
��10.0g��Ʒ��������������Ϊx����
Fe2O3 +3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
160 132
x 6.6g
$\frac{160}{x}$=$\frac{132}{6.6g}$
x=8g
��10.0g��Ʒ�к���������������Ϊ8.0g��
��Ʒ������������������Ϊ��$\frac{8g}{10g}$��100%=80%
��������ʯ��������������������80%��
���� ���⿼���˽������������˳���Ӧ�ã��ѶȲ�����ɴ��⣬�������ݽ������֪ʶ�����ش�

| A�� | ����������ˮ��������ɱ�� | |
| B�� | ��ù�Ĵ��������ɷ���ʳ�� | |
| C�� | ȱ��ά����A������ҹä֢ | |
| D�� | �̬��������ʯ�һ��ʹ�ÿ���������߷�Ч |
| ѡ�� | ʵ��Ŀ�� | ���� |
| A | ������������Һ���������Һ | ȡ�����μ�Ba��NO3��2��Һ���۲����� |
| B | ��������ˮ���Ȼ�����Һ | ȡ������Ʒ���μӵ�������ˮ���� |
| C | ��ȥ��ʯ���е�̼��� | �μ�����ֱ��û������ų� |
| D | ��ȥ�����е����������� | ���������顢�ܽ⡢���ˡ����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| ����װ�� | �ռ�װ�� | ���ƿ |
 | 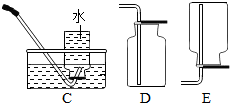 | 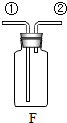 |
��2����ACװ�õ���Ͽ�����ȡ���ռ��������䷴Ӧ�Ļ�ѧ����ʽΪ2KClO3$\frac{\underline{MnO_2}}{��}$2KCl+3O2�������ó���ˮ�Ķ��װ��F�ռ�����ʱ��������Ӣڣ���١��ڡ�����ͨ�룮
��3��ʵ���ҿ���BDװ�õ������ȡ���ռ�������̼��������Ӧ�Ļ�ѧ����ʽΪCaCO3+2HCl=CaCl2+H2O+CO2����
��4����������ȡ������̼������Һ���������������IJ���ѵ��������������Ҫ��ͣ�ؽ��裬ֱ�����ֽ϶�������ʱ��д����ֹͣ���ȣ�
| A�� | NaOH NaCl KNO3 MgCl2 | B�� | NaOH NaCl HCl FeCl3 | ||
| C�� | Na2SO4 BaCl2 HCl K2CO3 | D�� | Na2CO3 HNO3 HCl Ba��NO3��2 |
| A�� | AlCl3 | B�� | Fe2��SO4��3 | C�� | MgCl2 | D�� | ZnSO4 |
 ͼΪijƷ��ţ�̵IJ��ֱ�ǩ����ݴ˻ش���������[�ڣ�2��-��4�����ñ�ǩ�е������д]��
ͼΪijƷ��ţ�̵IJ��ֱ�ǩ����ݴ˻ش���������[�ڣ�2��-��4�����ñ�ǩ�е������д]��
 2015��12�£���������������������ͨ������������Ҫ���Ĵ������������Ƚ�����
2015��12�£���������������������ͨ������������Ҫ���Ĵ������������Ƚ�����