题目内容
通过化学学 习,我们已经了解了常见金属在溶液中的活动性顺序。铬(Cr)是重要的金属材料,越来越受到人们的关注。某化学兴趣小组对Cr、Al、Cu的金属活动性顺序进行探究,过程如下:
习,我们已经了解了常见金属在溶液中的活动性顺序。铬(Cr)是重要的金属材料,越来越受到人们的关注。某化学兴趣小组对Cr、Al、Cu的金属活动性顺序进行探究,过程如下:
【提出假设】(1)对三种金属的活动性顺序提出三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c.
【设计实验】同温下,取大小相同的打磨过的金属薄片,分别投入到等体积等浓度的足量稀盐酸中,观察现象,记录如下:
| 金属 | Cr | Al | Cu |
| 与盐酸反应现象 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | 无气泡产生,金属无变化 |
【控制实验条件】(2)打磨三种金属发生的是 变化;上述实验使用等浓度的盐酸溶液的理由是 。
【得出结论】(3)原假设中正确的是 (填假设中“a”“b”或“c”)。写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式:
【结论应用】(4)根据探究结果,在CuCl2和AlCl3的混合液中加入一定量的金属铬,充分反应后过滤,向滤出的固体中加入盐酸,无明显现象,则滤液中一定含有的溶质是 。
(1)由于金属铝的活动性比铜强,故金属铬的活动性与金属铝和铜相比较,有以下三种情况:①Al>Cr>Cu;②Cr>Al>Cu;③Al>Cu>Cr。(2)打磨金属的过程中,只是金属的形状发生改变,由于没有新的物质生成,故属物理变化;比较金属活动性顺序的实验中,只是金属不同,而其他的方面如温度、酸的浓度都应当相同。(3)根据三种金属与酸是否反应以及与酸反应的剧烈程度,可得出它们的活动性顺序。(4)向滤出的固体中加入盐酸不发生反应,说明加入的金属铬完全反应,溶液中的氯化铜可能恰好完全反应,也可能有剩余,而原溶液中的AlCl3由于不能被金属铬置换,存在于滤液中。
答案:(1)Al>Cu>Cr (2)物理 盐酸的浓度不同,会影响反应产生的气体的速率
(3)a Cr+2H Cl====CrC
Cl====CrC l2+H2↑
l2+H2↑
(4)CrCl2、AlCl3

 环境保护是一个全球性的话题,作为对世界影响力最大的体育盛会--奥林匹克运动会,长期以来,在环保方面给世人留下的似乎是麻烦.2008年奥运,我国承诺“绿色奥运”.本次奥运会环保标志由人与绿树为主要形态.绿色的线条形如舞动的彩带,环绕交错,一笔描出,仿佛茂密的树冠,又似盛开的花朵,充满无限生机和希望,充分体现了自然环保的可持续性发展.树冠与人组成参天大树,代表着人与自然的和谐统一.
环境保护是一个全球性的话题,作为对世界影响力最大的体育盛会--奥林匹克运动会,长期以来,在环保方面给世人留下的似乎是麻烦.2008年奥运,我国承诺“绿色奥运”.本次奥运会环保标志由人与绿树为主要形态.绿色的线条形如舞动的彩带,环绕交错,一笔描出,仿佛茂密的树冠,又似盛开的花朵,充满无限生机和希望,充分体现了自然环保的可持续性发展.树冠与人组成参天大树,代表着人与自然的和谐统一.我们在初中化学学习的过程中接触了许多与环境保护有关的知识.
(一)空气污染与保护
(Ⅰ)二氧化碳是大气中的主要温室气体,我国二氧化碳的排放量位居世界第二.为减少空气中二氧化碳这种温室气体,我们可以采取的措施有(只填2种):
(Ⅱ)为减缓二氧化碳使全球变暖的趋势,有科学家提出大胆设想:将排放到空气中的二氧化碳压缩使其液化,然后将其压入到冰冷的深海中.但也有科学家担心海水中富含二氧化碳后酸度会增加,可能会杀死一些海洋生物,甚至会溶解掉部分海床,同时气候变化也可能改变海洋环流,把海底的二氧化碳又带回海面,另外把二氧化碳压入海底所消耗的能源可能会再增加二氧化碳的排放.
(1)实现二氧化碳液化,压缩过程将会
(2)二氧化碳使海水酸度增加的原理用化学方程式表示为:
(3)二氧化碳在深海中的溶解度
(二)水污染与保护
近几年我国不少水域多次发生“赤潮”、“水华”现象,这是水中的藻类生长繁殖过快导致的水质恶化现象.
(Ⅰ)河水的微生物使有机物(假设以C6H10O5表示)转化成二氧化碳和水的过程所需氧气的量叫生化需氧量(简称BOD),BOD是衡量水体质量的一个指标.写出C6H10O5和氧气反应的化学方程式
(Ⅱ)某化学兴趣小组在课外活动中,对某工厂排放出的无色废水进行了多次检测,其中三次检测结果如下表所示,请回答:
| 检测次数 | 废液中检测出的物质 |
| 第一次 | KNO3、Ba(NO3)2、Cu(NO3)2、HNO3 |
| 第二次 | KNO3、Ba(NO3)2、Mg(NO3)2、HNO3 |
| 第三次 | KNO3、Ba(NO3)2、AgNO3、HNO3 |
(2)在检测时,为了确定该工厂排放的废液中到底是否含有Mg2+、Ag+,该兴趣小组的同学作了进一步检验:取样,向其中加入
(3)加入适量的KOH,可以将废液中的Mg(NO3)2、HNO3除去,再加入适量的草木灰提取物(主要成分为碳酸钾,其余成分不参与反应),可以将废液中的Ba(NO3)2除去,并得到一种复合肥料,该复合肥料为
(4)为了防止废液中的钡离子污染环境,该兴趣小组提出了用草木灰提取物处理废水后再排放的建议.他们通过测定得知,该工厂排放出来的废水中Ba(NO3)2的质量分数为2.61%,已知该厂每天排放的废水为100吨,请通过计算确定每天需要多少吨K2CO3含量为30%的草木灰提取物,才能将废水中的钡离子除去?
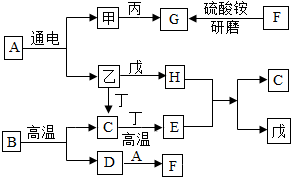 (2013?谷城县模拟)通过学习化学,我们了解了某些物质的性质以及物质之间的相互转化关系.如图中的物质均为初中化学常见的物质.其中甲、乙、丙、丁、戊均为单质,丙是空气中含量最多的物质;常温下,丁为黑色固体,戊为紫色金属;G是一种具有刺激性气味的气体,其水溶液显碱性,工业上用甲和丙化合制备G;农业上常用F改良土壤(如图中部分反应条件已省略).回答下列问题:
(2013?谷城县模拟)通过学习化学,我们了解了某些物质的性质以及物质之间的相互转化关系.如图中的物质均为初中化学常见的物质.其中甲、乙、丙、丁、戊均为单质,丙是空气中含量最多的物质;常温下,丁为黑色固体,戊为紫色金属;G是一种具有刺激性气味的气体,其水溶液显碱性,工业上用甲和丙化合制备G;农业上常用F改良土壤(如图中部分反应条件已省略).回答下列问题:
