题目内容
19.50℃时,NH4C1的溶解度为60g,50℃时,NH4Cl的饱和溶液中,溶质、溶 剂、溶液的质量比为( )| A. | 3:8:5 | B. | 3:5:8 | C. | 8:5:3 | D. | 8:3:2 |
分析 溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量;溶解度定义中的四要素:一定温度、100g溶剂、溶液达到饱和状态、溶解的质量及单位克.
解答 解:根据溶解度的概念,50℃时,NH4C1的溶解度为60g,其涵义是50℃时,100g水中最多溶解60gNH4C1,溶液达到饱和状态.则50℃时,NH4C1的饱和溶液中溶质、溶剂、溶液三者的质量比为60g:100g:(100g+60g)=3:5:8.
故选:B.
点评 本题难度不大,理解溶解度的概念,熟记溶解度的四要素(温度、100g溶剂、饱和状态、单位是克)是正确解答本题的关键.

练习册系列答案
相关题目
9.下列对应的化学方程式书写完全正确的是( )
| A. | 铁丝在氧气中燃烧:2Fe+3O2 $\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 硫在氧气中燃烧:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | |
| C. | 在密闭容器中燃烧红磷验证质量守恒定律:2P+O2$\frac{\underline{\;点燃\;}}{\;}$ P2O5 | |
| D. | 过氧化氢制取氧气:2H2O2═2H2O+O2↑ |
10.通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分得到粗盐.粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等).
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[资料准备]
[实验方案]某同学为了提纯粗盐,设计了如下实验方案并进行实验.

[交流与表达]
(1)实验步骤①和②的目的是除去粗盐中的难溶性杂质;实验步骤③和④的目的是除去粗盐中的易溶性杂质CaCl2、MgCl2.
(2)实验操作X的名称是过滤,该操作中要用到的玻璃仪器有烧杯、玻璃棒和漏斗.
(3)实验步骤③的主要目的是MgCl2+2NaOH═Mg(OH)2↓+2NaCl (用化学方程式回答);判断氢氧化钠溶液已过量的方法是取样品少许,加入试管中,滴加酚酞试液,溶液变红色.
(4)实验步骤④中生成的沉淀D是碳酸钙.(填写名称)
(5)实验步骤⑤用蒸发溶剂的方法而不用降低溶液温度的方法获取食盐晶体,原因是氯化钠的溶解度受温度影响较小;在蒸发食盐溶液的过程中要使用玻璃棒,作用是搅拌溶液,避免因局部过热,造成液滴飞溅.
[反思与评价]
(6)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中任意一种试剂就能将两种可溶性杂质出去,你认为这种方法不可行(选填“可行”或“不可行”),理由是MgCO3、Ca(OH)2均为微溶物,只用任意一种试剂就会有一种杂质生成微溶物而不能全部除去
(7)有同学认为原实验方案不完善,做出这种评价的依据是在除去MgCl2和CaCl2的同时,又引入了新的杂质NaOH和Na2CO3.
[实验方案设计]
(8)为了完善原实验方案,你设计的实验是向溶液C中逐滴加入稀盐酸至不再产生气泡,滴加酚酞试液时溶液不变色.(仅写出补充部分的实验操作和现象)
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[资料准备]
| 20℃时,一些物质的溶解度 | OH- | CO32- |
| Na+ | 溶 | 溶 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |

[交流与表达]
(1)实验步骤①和②的目的是除去粗盐中的难溶性杂质;实验步骤③和④的目的是除去粗盐中的易溶性杂质CaCl2、MgCl2.
(2)实验操作X的名称是过滤,该操作中要用到的玻璃仪器有烧杯、玻璃棒和漏斗.
(3)实验步骤③的主要目的是MgCl2+2NaOH═Mg(OH)2↓+2NaCl (用化学方程式回答);判断氢氧化钠溶液已过量的方法是取样品少许,加入试管中,滴加酚酞试液,溶液变红色.
(4)实验步骤④中生成的沉淀D是碳酸钙.(填写名称)
(5)实验步骤⑤用蒸发溶剂的方法而不用降低溶液温度的方法获取食盐晶体,原因是氯化钠的溶解度受温度影响较小;在蒸发食盐溶液的过程中要使用玻璃棒,作用是搅拌溶液,避免因局部过热,造成液滴飞溅.
[反思与评价]
(6)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中任意一种试剂就能将两种可溶性杂质出去,你认为这种方法不可行(选填“可行”或“不可行”),理由是MgCO3、Ca(OH)2均为微溶物,只用任意一种试剂就会有一种杂质生成微溶物而不能全部除去
(7)有同学认为原实验方案不完善,做出这种评价的依据是在除去MgCl2和CaCl2的同时,又引入了新的杂质NaOH和Na2CO3.
[实验方案设计]
(8)为了完善原实验方案,你设计的实验是向溶液C中逐滴加入稀盐酸至不再产生气泡,滴加酚酞试液时溶液不变色.(仅写出补充部分的实验操作和现象)
14. 如图是碳还原氧化铜的实验,有关说法正确的是( )
如图是碳还原氧化铜的实验,有关说法正确的是( )
 如图是碳还原氧化铜的实验,有关说法正确的是( )
如图是碳还原氧化铜的实验,有关说法正确的是( )| A. | 酒精灯加网罩的作用是防止火焰摆动 | |
| B. | 反应开始的标志是:导管口有气泡产生 | |
| C. | 反应结束的标志是:导管口不再产生气泡 | |
| D. | 实验结束时应先熄灭酒精灯,待试管冷却后再将导管从澄清石灰水中拿出 |
4.用分子的相关知识对下列现象或事实的解释不正确的是( )
| A. | 1滴水中大约有1.67×1021个水分子,说明分子很小 | |
| B. | 水沸腾时可掀起壶盖,说明分子大小随温度升高而增大 | |
| C. | 湿衣服晾在太阳下干得快,说明分子运动速率与温度有关 | |
| D. | 600 L氧气加压后可贮存在4 L钢瓶中,说明气体分子之间间隔较大 |
11.下列气体组中的各种气体都属于空气污染物的是( )
| A. | 二氧化硫 一氧化碳 二氧化氮 | B. | 二氧化碳 一氧化碳 氮气 | ||
| C. | 氧气 二氧化碳 氮气 | D. | 氮气 氧气 一氧化碳 |
8.某同学在探究学习活动中,测出了家中某些物质的pH:
(1)上述物质中能使紫色石蕊溶液变红的是醋.
(2)马蜂的蜂毒是酸性的,若你被马蜂蜇了,可用上述物质中的肥皂水、牙膏涂抹在皮肤上.
| 物质 | 醋 | 肥皂水 | 食盐水 | 牙膏 |
| pH | 3 | 10 | 7 | 9 |
(2)马蜂的蜂毒是酸性的,若你被马蜂蜇了,可用上述物质中的肥皂水、牙膏涂抹在皮肤上.
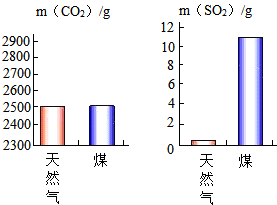 燃烧的知识不仅对保障生命财产安全非常重要,也对环境保护有着重要价值.
燃烧的知识不仅对保障生命财产安全非常重要,也对环境保护有着重要价值.