题目内容
14.三甲基一氯硅[(CH3)3SiCl]是一种生产有机硅化合物的原料,遇火能燃烧甚至会发生爆炸,与水接触可产生盐酸.则下列说法错误的是( )| A. | 保存三甲基一氯硅时应密封防水 | |
| B. | 三甲基一氯硅中碳氢元素质量比为4:1 | |
| C. | 三甲基一氯硅要严防明火或火花 | |
| D. | 三甲基一氯硅由碳、氢、硅、氯四个原子构成 |
分析 A、根据题意,三甲基一氯硅烷与水接触可产生盐酸,据此进行分析判断.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据题意,三甲基一氯硅烷与水接触可产生盐酸,遇明火会引起爆炸,据此进行分析判断.
D、根据三甲基一氯硅烷的微观构成进行分析判断.
解答 解:A、由题意,三甲基一氯硅烷与水接触可产生盐酸,则保存三甲基一氯硅烷时应密封防水,故选项说法正确.
B、三甲基一氯硅中碳、氢元素质量比为(12×3):(1×3×3)=4:1,故选项说法正确.
C、三甲基一氯硅烷与水接触可产生盐酸,遇明火会引起爆炸,三甲基一氯硅要严防明火或火花,故选项说法正确.
D、三甲基一氯硅烷是由三甲基一氯硅烷分子构成的,三甲基一氯硅烷分子是由碳、氢、硅、氯四种原子构成的,故选项说法错误.
故选:D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算等进行分析问题、解决问题的能力.

练习册系列答案
相关题目
4.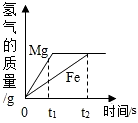 将一定质量的镁和铁分别放入相同质量、相同浓度的稀硫酸中,产生氢气的质量与反应时间的关系如图所示.下列说法中不正确的是( )
将一定质量的镁和铁分别放入相同质量、相同浓度的稀硫酸中,产生氢气的质量与反应时间的关系如图所示.下列说法中不正确的是( )
 将一定质量的镁和铁分别放入相同质量、相同浓度的稀硫酸中,产生氢气的质量与反应时间的关系如图所示.下列说法中不正确的是( )
将一定质量的镁和铁分别放入相同质量、相同浓度的稀硫酸中,产生氢气的质量与反应时间的关系如图所示.下列说法中不正确的是( )| A. | t1时,镁比铁产生氢气的质量大 | |
| B. | t1时,参加反应的镁与铁的总质量相等 | |
| C. | t2时,反应消耗稀硫酸的总质量一定相等 | |
| D. | 若加入的镁和铁的质量相等,反应结束后镁一定有剩余 |
5.下列实验操作叙述正确的是( )
| A. | 倾倒液体时,试剂瓶口紧挨着试管口快速倒入 | |
| B. | 加热蒸发过程中,当溶液蒸干时停止加热 | |
| C. | 过滤时,漏斗中液面低于滤纸的边缘 | |
| D. | 测溶液pH时,将试纸直接浸入待测溶液中,再与标准比色卡比较 |
2.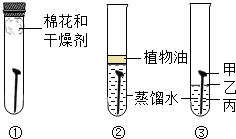 某学习小组用三只洁净无锈的铁钉对铁制品锈蚀条件进行探究,设计实验如图所示,一周后观察现象.下列说法错误的是( )
某学习小组用三只洁净无锈的铁钉对铁制品锈蚀条件进行探究,设计实验如图所示,一周后观察现象.下列说法错误的是( )
 某学习小组用三只洁净无锈的铁钉对铁制品锈蚀条件进行探究,设计实验如图所示,一周后观察现象.下列说法错误的是( )
某学习小组用三只洁净无锈的铁钉对铁制品锈蚀条件进行探究,设计实验如图所示,一周后观察现象.下列说法错误的是( )| A. | ①和②中铁钉无明显变化 | |
| B. | ②中加入的蒸馏水要事先煮沸,目的是除去水中溶解的二氧化碳 | |
| C. | ③中铁钉的甲、乙、丙三处,乙处锈蚀最严重 | |
| D. | 通过探究说明铁在潮湿空气中容易生锈 |
19.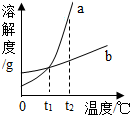 a,b两种物质的溶解度曲线如图所示.下列说法正确的是( )
a,b两种物质的溶解度曲线如图所示.下列说法正确的是( )
 a,b两种物质的溶解度曲线如图所示.下列说法正确的是( )
a,b两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | a物质的溶解度一定大于b物质的溶解度 | |
| B. | 将a溶液从t2℃时降温到t1℃时,一定有晶体析出 | |
| C. | t1℃时,a、b两种物质饱和溶液的溶质质量分数相等 | |
| D. | 将t2℃时b的饱和溶液变为不饱和溶液,可采取降温的方法 |
6.下列化学符号中的“2”表示的意义正确的是( )
| A. | H2:表示两个氢原子 | |
| B. | 2H:表示两个氢元素 | |
| C. | Mg2+:表示两个镁离子 | |
| D. | $\stackrel{+2}{Ca}O$:表示氧化钙中钙元素的化合价为+2价 |
 水是重要资源.
水是重要资源.