题目内容
20.通过一年的化学学习,相信你已经初步掌握了实验室制取气体及相关实验操作的有关知识.请结合图示回答问题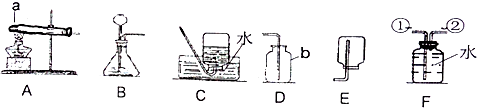
(1)实验室用装置B制取CO2时,如用注射器替换长颈漏斗,优点是可控制反应速率,又可节约药品.
(2)实验室加热氯酸钾制取氧气的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.若用盛满水的F装置收集氧气,应从导管②(填①或②)通入.
(3)氨气是一种有刺激性气味、易溶于水、密度比空气小的气体,实验室用加热氯化铵和熟石灰的固体混合物的方法制取氨气,则实验室制取氨气的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,实验室制取并收集氨气应选择的装置组合是A和E.
分析 (1)从注射器与长颈漏斗比较,注射器上有可以控制的活塞,可以根据实验时的需要控制添加药品的速度,故可控制反应速率,不用时可随时停止,又可节约药品去分析;
(2)根据加热氯酸钾和二氧化锰的混合物,生成氯化钾和氧气进行分析;根据氧气的密度比水小进行分析;
(3)从实验室用加热氯化铵和熟石灰的固体混合物的方法制取氨气,是加热固体制取气体;氨气易溶于水,密度比空气小去分析.
解答 解:(1)注射器与长颈漏斗比较,注射器上有可以控制的活塞,可以根据实验时的需要控制添加药品的速度,故可控制反应速率,不用时可随时停止,又可节约药品.
故答案为:可控制反应速率,又可节约药品;
(2)加热氯酸钾和二氧化锰的混合物,生成氯化钾和氧气,其化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;由于F装置内装满水,氧气的密度比水小,可从②进入,由于氧气不易溶于水,在氧气压力的不断增大下,集气瓶中的水会被压出,当水排净时,瓶内充满氧气.
故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑; ②;
(3)实验室制备氨气是利用氯化铵和氢氧化钙固体加热反应生成,反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;实验室用加热氯化铵和熟石灰的固体混合物的方法制取氨气,是加热固体制取气体,故发生装置应选择A;氨气易溶于水,所以不能用排水法收集,密度比空气小,所以可用向下排空气法收集;
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;A和E.
点评 实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度;考查了实验室制取氧气的反应原理,及注意事项,是考试的重点也是中考的重点.

| A. | 苹果醋饮料是混合物 | B. | 苹果酸不属于氧化物 | ||
| C. | 苹果酸属于无机化合物 | D. | 苹果酸属于有机物 |
| A. |  爱护花草树木 | B. |  随意排放废水 | C. |  分类回收垃圾 | D. |  绿色低碳出行 |
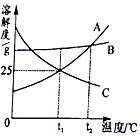
| A. | 物质A的溶解度大于物质C的溶解度 | |
| B. | A中含有少量B时,可以采用蒸发结晶提纯A | |
| C. | t2℃时,A、B、C三种物质的饱和溶液降温到t1℃,三种物质的质量分数大小为B>A=C | |
| D. | 将t1℃时,B、C两种物质的饱和溶液升温至t2℃,溶液中溶质质量分数不变的是B溶液 |
| A. | 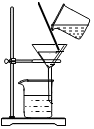 分离KNO3和NaCl | B. | 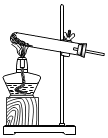 H2还原CuO | ||
| C. | 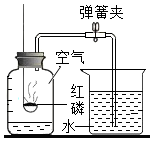 测定空气中氧气含量 | D. | 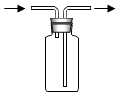 收集二氧化碳气体 |
| A. | 小宇同学推测气体是氢气并检验 | |
| B. | 小琪同学猜想CuCl2溶液呈酸性并测定 | |
| C. | 小寒同学认为气体是氨气并检验 | |
| D. | 小梁同学认为红色物质是铜并检验 |
| A. | HCl | B. | NaCl | C. | Na2CO3 | D. | KNO3 |