题目内容
4.写出下列反应的化学方程式,并在括号内注明基本反应类型:(1)过氧化氢溶液与二氧化锰混合制氧气2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;分解反应;
(2)工业上用赤铁矿炼铁Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)把镁条伸入二氧化碳的集气瓶中点燃会产生一种黑色固体和一种白色氧化物,写出此反应的化学方程式2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;置换反应.
分析 书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须依据客观事实、遵守质量守恒定律.只有熟悉四种基本反应类型的概念和特点,才能作出正确的判断.
解答 解:(1)用过氧化氢和二氧化锰制取氧气,反应物是过氧化氢,生成物是水和氧气,反应条件是二氧化锰作催化剂,方程式
为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;该反应符合“一变多”的特征,属于分解反应.
(2)一氧化碳和氧化铁反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)镁在二氧化碳中燃烧产生了白色粉末和黑色粉末,根据质量守恒定律可知,白色粉末是氧化镁,黑色粉末是碳,反应的化学方程式
为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
故答案为:(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;分解;(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(3)2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;置换;
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
14.在学习实验室制取二氧化碳时,小段同学查阅资料发现不能用浓盐酸做反应物制取二氧化碳,因为浓盐酸具有较强挥发性,挥发出氯化氢气体,会导致收集到的二氧化碳不纯(含有氯化氢气体);氯化氢气体溶于水就是盐酸(加热不易分解).
【提出问题】氯化氢( HCl)气体显酸性吗?氯化氢气体的水溶液盐酸显酸性吗?
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵紫色石蕊试剂染成的纸质干燥小花进行下图的三个实验:

【实验现象和结论】完成下列表格
【实验反思】某同学用石灰石和浓盐酸制取二氧化碳,将生成的气体通入紫色石蕊溶液中,溶液的颜色变化情况是D(填序号),原因是二氧化碳气体溶于水生成碳酸,浓盐酸挥发出的氯化氢气体进入溶液中形成盐酸,.短时间加热通入气体后的该溶液,溶液颜色变化情况是B(填序号).
A.变成紫色 B.不变色 C.变成无色 D.变成红色.
【提出问题】氯化氢( HCl)气体显酸性吗?氯化氢气体的水溶液盐酸显酸性吗?
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵紫色石蕊试剂染成的纸质干燥小花进行下图的三个实验:

【实验现象和结论】完成下列表格
| 实验Ⅰ | 实验Ⅱ | 实验Ⅲ | |
| 现象 | 小花不变红 | 小花不变红 | 小花变红 |
| 结论 | 水不显酸性 | 氯化氢气体不显酸性 | 氯化氢溶于水形成盐酸显酸性 |
A.变成紫色 B.不变色 C.变成无色 D.变成红色.
13.下列操作正确的是( )
| A. |  滴加液体 | B. | 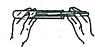 取用固体粉末 | C. |  闻气体的气味 | D. |  给液体加热 |