题目内容
6.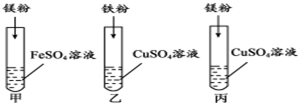 某化学活动小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案:
某化学活动小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案:乙试管中观察到的实验现象是(1)铁粉表面有红色的金属生成,溶液由蓝色逐渐变为浅绿色.同学们经过讨论得出三种金属的活动性由强到弱的顺序为(2)Mg、Fe、Cu请你评价该小组同学的实验设计(3)丙实验多余可不做试验后,小组同学将三支试管中的物质倒入同一大烧杯中,一段时间后过滤,得到不溶物和滤液,同学们对不溶物成分产生了浓厚的兴趣,进行了进一步的探究活动.
【提出问题】烧杯中不溶物的成分是什么?
【猜想与假设】A同学:铜 B同学:铜和铁 C同学:(4)镁、铜、铁.
分析 (1)根据金属的活动性顺序推测乙试管中的实验现象;(2)根据三个实验推测三种金属的活动性顺序;(3)根据实验目的结合三个实验分析设计情况进行评价;(4)根据金属的活动性进行判断.
解答 解:(1)在金属活动性顺序表中铁在铜的前面,所以铁可以和硫酸铜溶液发生反应置换出铜,故填:铁粉表面有红色的金属生成,溶液由蓝色逐渐变为浅绿色;(2)根据三个实验进行推断,甲实验可证明镁的活动性比铁强;乙实验可证明铁的活动性比铜强;丙实验可证明镁的活动性比铜强,故填:Mg、Fe、Cu;(3)根据(2)可看出甲、乙两个实验就可以推出三种金属的活动性强弱,故丙实验多余,故填:丙实验多余可不做;(4)由题中所给金属和发生的反应推断不溶物既为生成的金属或没反应完的金属,故三种金属如果只剩余一种一定是活动性最弱的铜,如果剩余两种则一定是活动性最弱的铜和次之的铁;还有可能三种都有剩余,故填:镁、铜、铁.
点评 本题考查了学生的实验设计能力,属于能力提高型习题,有一定的开放性,能培养学生分析实验评价实验的能力,掌握金属活动性顺序验证的原理是解题的关键.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
1.用分子的观点对下列现象的解释错误的是( )
| 选项 | 现象 | 解释 |
| A | 水结成冰后体积变大 | 分子间隔变大 |
| B | 破碎的玻璃无法复原 | 分子间存在斥力 |
| C | 闻到路边怡人的花香 | 分子不停地运动 |
| D | 两块表面平滑的铅块紧压后会结合起来 | 分子间存在引力 |
| A. | A | B. | B | C. | C | D. | D |
11.将H2、O2和N2的混合气体20g点燃,完全反应后生成18g水,下列情况中.不可能的是( )
| A. | 原混合气体中,H2的质量大于2g,同时氧气的质量小于16g | |
| B. | 原混合气体中,H2的质量大于2g,同时氧气的质量等于16g | |
| C. | 剩余的2g气体为N2 | |
| D. | 剩余的2g气体中含有H2、O2、N2 |
7.某化工厂用废硫酸制备K2SO4的流程如下:
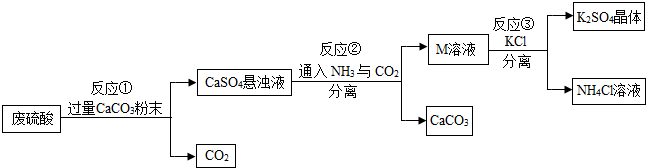
(1)生产上将CaCO3研成粉末的目的是加快反应速率,上述流程中,除可综合利用CO2外,还可循环使用的物质是CaCO3(填写化学式).
(2)M溶液的溶质主要成分是NH4Cl(填化学式).
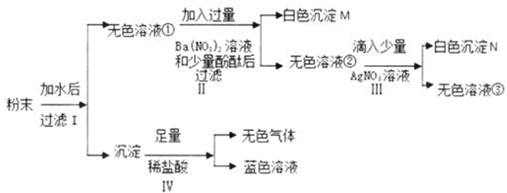
(3)洗涤反应③所得晶体不用水面用饱和K2SO4溶液的目的是减少K2SO4的溶解,检验此晶体是否洗涤干净的方法是取最后一次洗涤液,先加入过量的Ba(NO3)2溶液,振荡、静置,目的是除去硫酸根,再向上层清液中滴加AgNO3溶液,如果没有白色沉淀,说明洗涤干净.

| 物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
| 溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
(2)M溶液的溶质主要成分是NH4Cl(填化学式).
(3)洗涤反应③所得晶体不用水面用饱和K2SO4溶液的目的是减少K2SO4的溶解,检验此晶体是否洗涤干净的方法是取最后一次洗涤液,先加入过量的Ba(NO3)2溶液,振荡、静置,目的是除去硫酸根,再向上层清液中滴加AgNO3溶液,如果没有白色沉淀,说明洗涤干净.
4.下列有关食品中的化学知识的叙述不正确的是( )
| A. | 食盐可作调味剂,也可作食品防腐剂 | |
| B. | 新鲜蔬菜做热后,所含维生素C会有损失 | |
| C. | 油脂是人体的重要储能物质 | |
| D. | 淀粉和蛋白质都能在人体内与水作用生成葡萄糖,故为营养物质 |
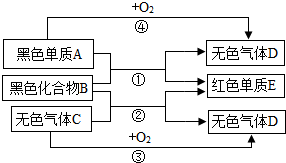 A是非金属,E是金属,B、C、D是化合物,它们之间有如图所示的转化关系(反应条件已略去):
A是非金属,E是金属,B、C、D是化合物,它们之间有如图所示的转化关系(反应条件已略去):