题目内容
(8分)溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。
(1)厨房中的下列物质加入水中,能形成溶液的有 (填编号);
a.面粉 b.食盐 c.白糖 d.牛奶
(2)下图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线。

①t2℃时,甲的溶解度 (填“>”、“<”或“=”)乙的溶解度;
②t1℃时,将50克的甲加入到100克的水中,充分搅拌后所得溶液的质量为 克;
③将t1℃时甲的饱和溶液升高温度到t2℃(假设水分没有蒸发),则与原溶液相比,所得溶液中溶质的质量分数将 (填“变大”、“变小”或“不变”);
④将t2℃时,甲、乙两种物质相同质量的饱和溶液,分别冷却到t1℃,析出晶体最多的是 物质。
(3)气体的溶解度也有一定的变化规律。
①打开可乐瓶,逸出大量气泡。由此可见,压强越小,CO2的溶解度越 。为增大CO2的溶解度,可采用的一种方法是 。
②不同温度下,氧气的溶解度随压强的变化如图所示,
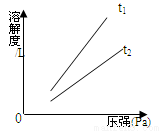
图中t1对应的温度为40℃,则t2对应的温度 (填编号)。
a.大于40℃ b.小于40℃ c.无法确定
(1)bc (2)①> ②140克 ③不变 ④甲(3)①小;降低温度或增加压强 ②a
【解析】
试题分析:能够形成溶液首先必须能溶解在对应的溶剂内,t1℃时甲的溶解度为40克,所以100克水在该温度只能溶解40克甲,所以溶液的质量为140克,将t1℃时甲的饱和溶液升高温度到t2℃,水分没有蒸发,溶解度变大,不会有溶质洗出,所以溶液没有变化,甲的溶解度受温度影响大,所以改变温度甲洗出的晶体会多,气体的溶解度受压强和温度的影响,压强越大溶解度越大,温度越低溶解度越大。
考点:溶解度及其曲线的认识 溶液的形成

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的应用
(1)下列铁制品的利用与金属导热性有关的是 (填字母,下同)。
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的 。
Ⅱ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式: ;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能 ;
Ⅲ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4  CO↑+ CO2↑+ H2O。
CO↑+ CO2↑+ H2O。
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;

于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的 (填装置编号);

(2)图中装置C、D的作用分别是 、 ;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的 (填试剂名称),反应的化学方程式为 ;
(4)该装置设计有一个明显缺陷,你认为是 。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。
b. Fe2O3与CO反应的固体生成物可能情况如下:

根据“无气泡”猜想,黑色粉末可能是:① Fe3O4 ;② ③ 。
(6)定量分析 用电子天平称量得部分数据如下:
玻璃管质量 | 玻璃管及其中固体的质量 | 装置F及其中物质的总质量 | |
反应前 | 28.20 g | 33.00 g | 300.0 g |
反应后 | 32.84 g | 300.4 g |
根据上述数据,纯净的Fe2O3固体质量为 g,请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程) 。
根据推断结果,写出该实验中玻璃管内发生的化学反应方程式:

