题目内容
14.向盛有10g氧化铜的玻璃管通一会儿CO后,进行加热,一段时间后,试管内残渣为9.6g,残渣中铜元素的质量分数最接近的是( )| A. | 81.1% | B. | 83.3% | C. | 85.5% | D. | 96% |
分析 根据质量守恒定律反应前后元素的质量相等;残渣中铜元素的质量即为氧化铜中铜元素的质量,根据氧化铜的质量可求得铜元素的质量,进一步可求得残渣中铜元素的质量分数.
解答 解:氧化铜与一氧化碳在加热条件下生成铜和二氧化碳,加热一段时间,氧化铜不一定完全转化成铜,因此9.6g残渣不一定是生成的铜的质量,可能是生成的铜和剩余的氧化铜的混合物.根据质量守恒定律反应前后元素质量不变;残渣中铜元素的质量即为氧化铜中铜元素的质量.
10克残渣中铜元素的质量为:10g×$\frac{64}{64+16}$=8g,
9.6g残渣中铜元素的质量分数为:$\frac{8g}{9.6g}$×100%≈83.3%.
故选B.
点评 本题重点是考虑到元素质量守恒,反应前后元素的质量相等,问题就很简单了,很容易求得铜元素的质量.

练习册系列答案
相关题目
4.下列关于物质的组成、结构、性质以及变化规律的总结中,正确的是( )
| A. | Cl、Cl-两种粒子的质子数相同,化学性质相同 | |
| B. | NaHCO3、HCl的组成中都含有氢元素,溶液都显酸性 | |
| C. | 构成金刚石和石墨的碳原子排列方式不同,金刚石和石墨的化学性质一定不同 | |
| D. | H2、CO都能与灼热CuO反应生成铜,在加热条件下H2、CO都具有还原性 |
5.已知M、N在一定条件下,能发生反应:M+2N═P+2Q,则下列说法中不正确的是( )
| A. | 若M、N、P、Q都是由分子构成的物质,则该反应前后分子的数目一定不变 | |
| B. | M、N、P、Q可能含有同一种元素 | |
| C. | 若P、Q都是化合物,则该反应一定是复分解反应 | |
| D. | 若16 g M和64 g N能恰好完全反应,则M、N的相对分子质量之比为1:4 |
2.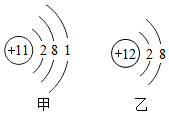 下列关于甲、乙两种粒子的结构示意图的说法中不正确的是( )
下列关于甲、乙两种粒子的结构示意图的说法中不正确的是( )
 下列关于甲、乙两种粒子的结构示意图的说法中不正确的是( )
下列关于甲、乙两种粒子的结构示意图的说法中不正确的是( )| A. | 甲乙两种微观粒子属于不同种元素 | |
| B. | 粒子甲是原子,粒子乙是阳离子 | |
| C. | 粒子甲表示的元素在化合物中通常显-1价 | |
| D. | 粒子乙的结构是稳定结构 |
19.下列成语涉及化学变化的是( )
| A. | 百炼成钢 | B. | 香气四溢 | C. | 木已成舟 | D. | 水乳交融 |
6.如图各物质均为初中化学常见的物质(反应条件省略),下列说法正确的是( )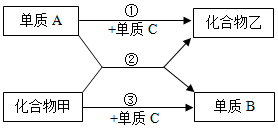

| A. | 常温下,化合物乙一定是无色气体 | B. | 化合物甲可能含有3种元素 | ||
| C. | 反应②一定是置换反应 | D. | 单质B一定是金属铜 |
5.下列关于a、b数值的比较中,a一定小于b的是( )
| A. | 不饱和溶液中溶质的质量分数为a%,饱和溶液中溶质的质量分数为b% | |
| B. | 同一饱和溶液中,溶质的质量分数为a%,溶解度为b克 | |
| C. | 某物质的饱和溶液中溶质的质量分数为a%,向其中加入少量该物质后,溶质的质量分数为b% | |
| D. | 某物质的溶解度在低温时为a克,高温时为b克 |