题目内容
某混合气体中可能含有氢气、一氧化碳、二氧化碳的一种或几种.把混合气体通入灼热的盛有足量氧化铜的试管(已排尽空气),充分反应后,管内固体质量减少1.6g,将反应完全后的气体全部通入过量的澄清石灰水,充分反应后,得到10g白色沉淀,则混合气体的组成可能的是.
| A、一氧化碳 |
| B、氢气和一氧化碳 |
| C、二氧化碳和氢气 |
| D、氢气、一氧化碳、二氧化碳 |
考点:常见气体的检验与除杂方法,根据化学反应方程式的计算
专题:物质的检验、鉴别与推断
分析:根据质量守恒定律可知,将反应后的气体全部通入过量的澄清石灰水中,充分反应后得到10g白色沉淀,说明通过过量灼热的Cu0的试管后二氧化碳的质量为4.4g,所以气体X是一氧化碳,则试管内物质减少的质量恰好与题目中给出的数据相等由此推知气体的成分进行解答.
解答:解:由质量守恒定律可知,将反应后的气体全部通入过量的澄清石灰水中,充分反应后得到10g白色沉淀,说明通过过量灼热的Cu0的试管后二氧化碳的质量为4.4g,所以气体X是一氧化碳,则试管内物质减少的质量恰好与题目中给出的数据相等由此推知气体的成分可能是一氧化碳或氢气和二氧化碳或一氧化碳、二氧化碳、氢气,而不可能是一氧化碳、氢气,因为若氢气和一氧化碳共同还原氧化铜,使管内物质质量减少1.6g,那么生成的二氧化碳的质量将小于4.4g,通入过量的澄清石灰水中,充分反应后得到白色沉淀的质量一定小于10g.
故选:B.
故选:B.
点评:本题重在考查CO2、CO、H2化学性质,并在掌握化学性质的基础上灵活运用的能力,并且要灵活运用质量守恒定律和有关化学方程式的计算.

练习册系列答案
相关题目
下列物质在氧气中燃烧产生明亮蓝紫色火焰的是( )
| A、红磷 | B、木炭 | C、铁丝 | D、硫 |
走进化学实验室,同学们学会了最基本的实验操作.以下基本操作数据合理正确的是( )
A、 用滴管吸取2mL溶液 |
B、 用量筒量取45mL水 |
C、 用托盘天平称取7.5g食盐 |
D、 用广泛pH试纸测得某溶液的pH为2.5 |
根据化学方程式,无法获得的信息是( )
| A、该反应的反应物和生成物 |
| B、各反应物和生成物的质量比 |
| C、该反应所需要的条件 |
| D、该化学反应速率的快慢 |
 实验室按如图所示装置制取CO2,并检验CO2的性质,试回答以下问题.
实验室按如图所示装置制取CO2,并检验CO2的性质,试回答以下问题.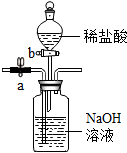 如图所示,装置a为弹簧夹,b为分液漏斗的活塞(通过开、关活塞可以随时滴加液体).先关闭b,打开a,将混有少量CO的CO2气体由左侧导管通入,充分反应后,排出的气体主要是
如图所示,装置a为弹簧夹,b为分液漏斗的活塞(通过开、关活塞可以随时滴加液体).先关闭b,打开a,将混有少量CO的CO2气体由左侧导管通入,充分反应后,排出的气体主要是 扎西同学准备进行常见酸、碱、盐的性质实验时,发现实验台上有一瓶标签破损的溶液(如图),已知它是氯化钠溶液、氢氧化钠溶液、碳酸钠溶液三者中的一种,于是决定对这瓶溶液进行实验探究.
扎西同学准备进行常见酸、碱、盐的性质实验时,发现实验台上有一瓶标签破损的溶液(如图),已知它是氯化钠溶液、氢氧化钠溶液、碳酸钠溶液三者中的一种,于是决定对这瓶溶液进行实验探究.