题目内容
11. 小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:
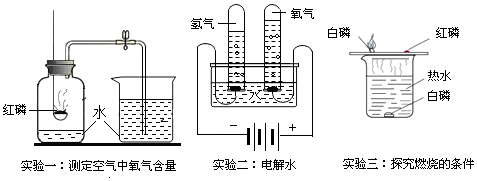
小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:第一组实验:取5只集气瓶,编号为①、②、③、④、⑤,分别装入其总容积10%、20%、30%、40%、50%的水.用排水法收集氧气,恰好把5只集气瓶中的水排去.将带火星的木条依次插入①~⑤号瓶中,记录实验现象.
小亮在前一组实验的基础上又做了第二组和第三组实验,三组实验的数据和现象见下表.
| 第一组 | 第二组 | 第三组 | |||||||||
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| 收集的O2占容积的体积分数(%) | l0 | 20 | 30 | 40 | 50 | 3l | 33 | 35 | 37 | 39 | 34 |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
(1)使用带火星的木条验满氧气的方法是否可靠:否(填“是”或“否”).
(2)集气瓶中氧气的体积分数=收集的氧气占容积的体积分数+瓶中空气占容积的体积分数×21%.
(3)收集的氧气占容积的体积分数最低为35%时,可使带火星的木条复燃,这时集气瓶中氧气分数是49%(计算结果保留整数).
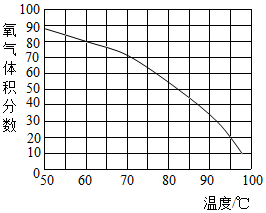
(4)用带火星的木条直接检验双氧水受热分解产生的氧气时,往往难以复燃,这是因为在加热生成氧气的同时产生大量水蒸汽所致,此时混合气体中氧气的体积分数随温度变化的曲线如右下图所示.若只考虑氧气的体积分数对实验结果的影响,欲使带火星的木条复燃,应将加热双氧水的最高温度控制在82℃.
(5)采取“半值法”探究能减少实验次数.例如:第一组实验若按③、④的编号顺序进行实验,即可确定下一组实验收集的氧气占容积的体积分数应在30%~40%之间,从而省去编号为①、②、⑤的实验.同理,第二组实验可以省去的实验编号为①、④、⑤.
(6)氧气可用排水法收集,这是因为不易溶于水.
分析 (1)根据带火星的木条复燃时氧气的体积的以及分数分析;
(2)根据空气中氧气的体积分数分析;
(3)根据木条复燃时氧气的体积分数和空气中氧气的体积分数分析计算;
(4)根据集气瓶中氧气复燃的体积分数查出应将加热双氧水控制的最高温度;
(5)根据“半值法”探究实验的方法分析第二组实验可以省去的实验;
(6)根据氧气的溶解性分析回答.
解答 解:(1)通过实验可以看出,氧气含量达到35%带火星的木条就可以复燃,所以用带火星的木条验满氧气的方法不可靠;
(2)集气瓶中氧气的体积分数=收集的氧气占容积的体积分数+瓶中空气占容积的体积分数×21%.
(3)由图中可知,当氧气的体积分数达到35%时,带火星的木条复燃,即收集的氧气占容积的体积分数最低为35%,此时空气还占65%,所以空气中含有氧气的以及分数为:65%×21%≈14%,所以此时瓶内共有氧气的分数为14%+35%=49%;
(4)只考虑氧气的体积分数对实验结果的影响,欲使带火星的木条复燃,则氧气的含量需要在图3坐标中的49%处,向横坐标作垂线,则可知温度大约在82℃左右.
(5)采取“半值法”探究能减少实验次数,实际上就是通过实验数据的分析,减少不必要的实验,第二组实验若按②、③的编号顺序进行实验,即可确定下一组实验收集的氧气占容积的体积分数应在33%~35%之间,从而省去编号①、④、⑤的实验;
(6)氧气可用排水法收集,这是因为不易溶于水.
故答案为:(1)否;(2)21;(3)35,49;(4)82;(5)①、④、⑤;(6)不易溶于水.
点评 设计实验时,要明确实验的目的,要注意控制一些变量,本题还采用了“半值法”,从而可减少实验的次数,减少实验的过程.

练习册系列答案
相关题目
1.下列有关碳单质所发生的变化中,属于化学变化的是( )
| A. | 以石墨为原料制造人造金刚石 | |
| B. | 用铅笔芯在纸上写字,铅笔芯变短了 | |
| C. | 将金刚石加工琢磨成钻石 | |
| D. | 将活性炭投入紫色石蕊溶液中,最终溶液变为无色 |
2.维生素C是生命活动中不可缺少的物质,不同的饮料中维生素C的含量不同.下面是小明同学运用学到的实验方法测定(比较)橙汁、果味饮料中维生素C含量的实验方案与结果.
测定不同饮料中维生素C的含量.
(1)维生素C是一种无色的易溶于水的有机物,能够和碘水反应.
(2)淀粉遇到碘水变蓝色.
碘水、淀粉溶液、已知浓度的标准维生素C溶液、蒸馏水.
步骤(Ⅰ)在4支试管中分别盛有3mL下列物质:①蒸馏水;②标准维生素C溶液;③橙汁;④果味饮料.分别向4支试管中滴加2滴淀粉液.
步骤(Ⅱ)用胶头滴管向①试管中滴加1滴碘水,试管中物质变蓝色.
步骤(Ⅲ)按相同的操作方法向②中滴加1滴碘水,振荡试管,再加1滴碘水,再振荡试管,重复上述操作至试管中物质刚好变成蓝色为止.记录向②试管中加入碘水的滴数.
步骤(Ⅳ)对于③、④试管中样品,重复步骤(Ⅲ)的操作.
试回答以下问题:
(1)你认为小明测定的两种饮料中,哪一种维生素C含量较高?橙汁.
(2)化学实验需要控制变量.下列哪些情况会影响到测定结果?BC.
A、试管的大小不同 B、量取的被测试物质的体积不同
C、没有用同一规格胶头滴管按相同的操作方法向③、④中滴加碘水
(3)有人认为测定物质②是多余的,你认为呢?请说明理由.不是多余的.通过①②的实验对比,可以获得维生素C和单质碘反应时的数量比,根据该数量比和实验③④测得的数据计算出橙汁、该果味饮料维生素C含量.
测定不同饮料中维生素C的含量.
(1)维生素C是一种无色的易溶于水的有机物,能够和碘水反应.
(2)淀粉遇到碘水变蓝色.
碘水、淀粉溶液、已知浓度的标准维生素C溶液、蒸馏水.
步骤(Ⅰ)在4支试管中分别盛有3mL下列物质:①蒸馏水;②标准维生素C溶液;③橙汁;④果味饮料.分别向4支试管中滴加2滴淀粉液.
步骤(Ⅱ)用胶头滴管向①试管中滴加1滴碘水,试管中物质变蓝色.
步骤(Ⅲ)按相同的操作方法向②中滴加1滴碘水,振荡试管,再加1滴碘水,再振荡试管,重复上述操作至试管中物质刚好变成蓝色为止.记录向②试管中加入碘水的滴数.
步骤(Ⅳ)对于③、④试管中样品,重复步骤(Ⅲ)的操作.
| 测定物质 | 滴入碘水的数量(滴) |
| ①蒸馏水 | 1 |
| ②标准维生素C溶液 | 8 |
| ③橙汁 | 15 |
| ④果味饮料 | 5 |
(1)你认为小明测定的两种饮料中,哪一种维生素C含量较高?橙汁.
(2)化学实验需要控制变量.下列哪些情况会影响到测定结果?BC.
A、试管的大小不同 B、量取的被测试物质的体积不同
C、没有用同一规格胶头滴管按相同的操作方法向③、④中滴加碘水
(3)有人认为测定物质②是多余的,你认为呢?请说明理由.不是多余的.通过①②的实验对比,可以获得维生素C和单质碘反应时的数量比,根据该数量比和实验③④测得的数据计算出橙汁、该果味饮料维生素C含量.
20.铜、铁是人类使用最早、应用广泛的金属.
(一)对古代制品的认识
青铜铸件、丝绸织品、陶瓷器皿是我国古代劳动人民创造的辉煌成就.
1、上述制品不涉及到的材料是C(选填序号).
A、金属材料 B、无机非金属材料 C、复合材料
(2)如图1为出土文物古代青铜铸件“马踏飞燕”.该文物能保存至今的原因可能是AC(选填序号).
A、铜的活泼性弱 B、铜不会生锈 C、深埋于地下,隔绝空气
(二)铁、铜的冶炼
1、我国古代曾用孔雀石炼铜,涉及主要反应的化学方程式:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑+2CuO,2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
2、铁、铜矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2)、黄铜矿(CuFeS2)等.CuFeS2为二硫化亚铁铜,其中S元素的化合价为-2.
(1)工业炼铁大多采用赤铁矿、磁铁矿.以磁铁矿为原料炼铁反应的化学方程式为Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.炼铁不采用黄铁矿、黄铜矿,可能的原因是:
①黄铁矿、黄铜矿含铁量相对低;②冶炼过程中会产生有毒气体二氧化硫,污染环境.
(2)以黄铜矿为原料,采用生物炼铜是现代炼铜的新工艺,原理为:4CuFeS2+17O2+2H2SO4$\frac{\underline{\;耐酸、铜细菌\;}}{\;}$4CuSO4+2Fe2(SO4)3+2H2O.
向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu.
①发生主要反应的化学方程式:Fe+Fe2(SO4)3=3FeSO4,Fe+CuSO4=Cu+FeSO4.
②FeSO4溶液经蒸发浓缩、降温结晶、过滤等操作得到FeSO4•7H2O晶体.
(三)黄铜矿中铁、铜含量的测定
在科研人员指导下,兴趣小组称取25.00g黄铜矿(含少量Fe2O3和其它不含金属元素的杂质)模拟生物炼铜,使其全部转化为CuSO4、Fe2(SO4)3溶液.向溶液中加入过量NaOH溶液得到Cu(OH)2、Fe(OH)3固体.
1、证明NaOH溶液过量的方法:静置,向上层清液中滴加NaOH溶液,无现象.
2、用图2装置对固体进行热分解实验.
【资料】
①在68℃时,Cu(OH)2分解为CuO;在500℃时,Fe(OH)3分解为Fe2O3.
②在1400℃时,CuO分解为Cu2O和O2,Fe2O3分解为复杂的铁的氧化物和O2.
(1)装配好实验装置后,先要检查装置的气密性.
(2)停止加热后仍需继续通N2,可防止倒吸和使生成的气体全部被B和C装置吸收.
(3)控制不同的温度对A中固体加热,测得装置B和C中铜网的质量变化如表.
①此黄铜矿中铜、铁元素的质量分数:ω(Cu)%=25.60%;ω(Fe)%=26.88%.
②复杂的铁的氧化物化学式为Fe4O5.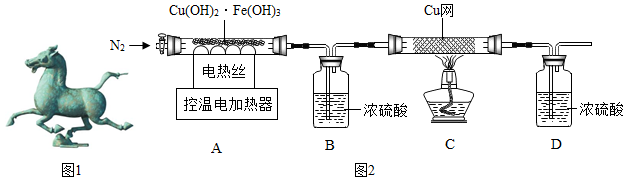
(一)对古代制品的认识
青铜铸件、丝绸织品、陶瓷器皿是我国古代劳动人民创造的辉煌成就.
1、上述制品不涉及到的材料是C(选填序号).
A、金属材料 B、无机非金属材料 C、复合材料
(2)如图1为出土文物古代青铜铸件“马踏飞燕”.该文物能保存至今的原因可能是AC(选填序号).
A、铜的活泼性弱 B、铜不会生锈 C、深埋于地下,隔绝空气
(二)铁、铜的冶炼
1、我国古代曾用孔雀石炼铜,涉及主要反应的化学方程式:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑+2CuO,2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
2、铁、铜矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2)、黄铜矿(CuFeS2)等.CuFeS2为二硫化亚铁铜,其中S元素的化合价为-2.
(1)工业炼铁大多采用赤铁矿、磁铁矿.以磁铁矿为原料炼铁反应的化学方程式为Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.炼铁不采用黄铁矿、黄铜矿,可能的原因是:
①黄铁矿、黄铜矿含铁量相对低;②冶炼过程中会产生有毒气体二氧化硫,污染环境.
(2)以黄铜矿为原料,采用生物炼铜是现代炼铜的新工艺,原理为:4CuFeS2+17O2+2H2SO4$\frac{\underline{\;耐酸、铜细菌\;}}{\;}$4CuSO4+2Fe2(SO4)3+2H2O.
向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu.
①发生主要反应的化学方程式:Fe+Fe2(SO4)3=3FeSO4,Fe+CuSO4=Cu+FeSO4.
②FeSO4溶液经蒸发浓缩、降温结晶、过滤等操作得到FeSO4•7H2O晶体.
(三)黄铜矿中铁、铜含量的测定
在科研人员指导下,兴趣小组称取25.00g黄铜矿(含少量Fe2O3和其它不含金属元素的杂质)模拟生物炼铜,使其全部转化为CuSO4、Fe2(SO4)3溶液.向溶液中加入过量NaOH溶液得到Cu(OH)2、Fe(OH)3固体.
1、证明NaOH溶液过量的方法:静置,向上层清液中滴加NaOH溶液,无现象.
2、用图2装置对固体进行热分解实验.
【资料】
①在68℃时,Cu(OH)2分解为CuO;在500℃时,Fe(OH)3分解为Fe2O3.
②在1400℃时,CuO分解为Cu2O和O2,Fe2O3分解为复杂的铁的氧化物和O2.
(1)装配好实验装置后,先要检查装置的气密性.
(2)停止加热后仍需继续通N2,可防止倒吸和使生成的气体全部被B和C装置吸收.
(3)控制不同的温度对A中固体加热,测得装置B和C中铜网的质量变化如表.
| 温度/℃ | 室温 | 100 | 550 | 1400 |
| B装置/g | 200.00 | 201.80 | 205.04 | 205.04 |
| C中铜网/g | 100.00 | 100.00 | 100.00 | 101.28 |
②复杂的铁的氧化物化学式为Fe4O5.

1.下列各组离子在溶液中能大量共存的是( )
| A. | H+、Cl-、OH-、Na+ | B. | H+、Ca2+、SO42-、HCO3- | ||
| C. | Ba2-、H+、Cl-、SO42- | D. | Cu2+、Na+、Cl-、SO42- |