题目内容
5. 盐酸是一种重要的化工产品,也是实验室中重要的化学试剂.
盐酸是一种重要的化工产品,也是实验室中重要的化学试剂.(1)增大压强,HC1由气态变为液态,从微观的角度分析该变化过程中改变的是氯化氢分子之间的间隔.
(2)在盐酸中加入过量的铁粉充分反应.
①可以看到的现象是有气泡产生,溶液由无色变为浅绿色.
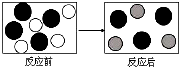
②如图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):
 H+,
H+, Cl-,
Cl-, Fe2+.
Fe2+.③下列金属中能与盐酸发生类似反应的是BC(填选项).
A.Cu B.Mg C.Al D.Ag.
分析 (1)增大压强,HC1由气态变为液态,属于物理变化,据此结合分子的基本性质,进行分析解答.
(2)①根据铁与稀盐酸反应生成氯化亚铁溶液和氢气,进行分析解答.
②在盐酸中加入过量的铁粉充分反应,
③在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,进行分析解答.
解答 解:(1)增大压强,HC1由气态变为液态,属于物理变化分子本身没有发生改变,改变的是氯化氢分子之间的间隔.
(2)①铁和稀盐酸反应生成氯化亚铁溶液和氢气,可以看到有气泡产生,溶液由无色变为浅绿色.
②反应前,溶液中含有大量的氢离子、氯离子;反应后,溶液中含有大量的氯离子、亚铁离子;反应后氢离子消失、氯离子不变,有亚铁离子生成,故三种离子分别为:H+、Cl-、Fe2+.
③在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,镁和铝能与稀盐酸反应.
故答案为:(1)氯化氢分子之间的间隔;
(2)①有气泡产生,溶液由无色变为浅绿色;②H+、Cl-、Fe2+;③BC.
点评 本题难度不大,熟练掌握酸的化学性质、分子的基本性质、金属的化学性质是正确解答本题的关键.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
15.工业上常利石灰浆[主要成分为Ca(OH)2]制备化工原料KClO3和超细CaCO3.
Ⅰ.制备KClO3的流程如图:

已知:①反应1为:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O.
②有关物质在常温下的溶解度如表:
(1)操作a的名称是过滤,在实验室中完成此操作需要的玻璃仪器有烧杯、玻璃棒、漏斗,该操作中玻璃棒的作用是引流.
(2)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和KClO3(填化学式),你认为该反应能得到KClO3晶体的原因是氯酸钾在该温度下的溶解度小.
(3)洗涤KClO3晶体时,可选用下列BC洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如图已知NH4Cl溶液呈酸性.
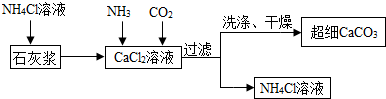
(1)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.该流程可循环使用的物质是NH4Cl.
(2)检验CaCO3是否洗涤干净的方法是:取最后一次洗涤液,向其中滴加AB(填写序号),观察,根据实验现象推断是否洗干净.
A.Na2CO3溶液 B.AgNO3溶液 C.酚酞试液.
Ⅰ.制备KClO3的流程如图:

已知:①反应1为:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O.
②有关物质在常温下的溶解度如表:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(2)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和KClO3(填化学式),你认为该反应能得到KClO3晶体的原因是氯酸钾在该温度下的溶解度小.
(3)洗涤KClO3晶体时,可选用下列BC洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如图已知NH4Cl溶液呈酸性.

(1)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.该流程可循环使用的物质是NH4Cl.
(2)检验CaCO3是否洗涤干净的方法是:取最后一次洗涤液,向其中滴加AB(填写序号),观察,根据实验现象推断是否洗干净.
A.Na2CO3溶液 B.AgNO3溶液 C.酚酞试液.
20.化学实验过程中一定要注意安全,万一发生事故也不必惊慌,要冷静地处理.下列做法不正确的是( )
| A. | 不慎将水银温度计打碎洒落在桌面上,立即扫入垃圾桶中 | |
| B. | 不慎将酒精灯碰倒,洒出的酒精在桌上燃烧起来,立刻用湿布扑灭 | |
| C. | 不慎将浓硫酸沾到皮肤上,立刻用大量水冲洗,再涂上3%一5%碳酸氢钠溶液 | |
| D. | 不慎将氢氧化钠溶液沾到皮肤上,立刻用大量水冲洗,再涂上硼酸溶液 |
10.学习化学帮助我们形成更好的生活方式,下列说法不正确的是( )
| A. | 食用蔬菜和水果可以补充维生素C | |
| B. | CO(NH2)2属于复合肥 | |
| C. | 地沟油经过化学方法的处理形成航空燃油,实现了变废为宝 | |
| D. | 用灼烧的方法区别棉花和羊毛 |