题目内容
4.某同学为了测定某种黄铜中铜、锌的质量分数进行了如下实验:将这种黄铜粉碎处理后称取10g,置于盛有100g稀硫酸(足量)的烧杯中,充分反应后测得烧杯中各物质的总质量为109.9g,请回答下列问题:(1)反应后得到氢气的质量为0.1g;
(2)通过计算求出黄铜中铜的质量分数.
分析 (1)根据金属的活动性Zn>H>Cu可知,黄铜中铜不能与稀硫酸反应,而锌可与稀硫酸反应放出氢气,因此,根据质量守恒定律,恰好完全反应前后的质量差即为反应放出氢气的质量;
(2)根据反应的化学方程式,可利用生成氢气的质量计算出锌的质量,即可求合金中铜质量分数.
解答 解:(1)根据质量守恒定律,反应生成的氢气质量为:10g+100g-109.9g=0.1g;
(2)设反应生成的氢气0.1g,参与反应的锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.1g
$\frac{65}{x}=\frac{2}{0.1g}$
解得 x=3.25g
合金中铜的质量分数为:$\frac{10g-3.25g}{10g}$×100%=67.5%.
答:(1)0.1;(2)黄铜中铜的质量分数是67.5%;
点评 利用质量守恒定律,根据反应前后质量差计算出放出氢气质量为解决问题的出发点.

练习册系列答案
相关题目
14.下列物质中属于纯净物的是( )
| A. | 蒸馏水 | B. | 煤 | C. | 青铜马 | D. | 金镶玉 |
12.下列化学用语中,正确的是( )
| A. | 2个氧分子:2O | B. | 2个镁离子:2Mg2+ | C. | 二氧化氮:N2O | D. | 硫酸铝:AlSO4 |
19.物质的用途与性质密切相关,下列说法不正确的是( )
| A. | 铜用于做导线,是由于铜有优良的导电性 | |
| B. | 氮气常用作保护气,是由于氮气的化学性质活泼 | |
| C. | 二氧化碳用于灭火,是由于二氧化碳不可燃、不助燃 | |
| D. | 氧气可用于登山,是由于氧气可供给呼吸 |
9.下列说法正确的是( )
| A. | 人体缺乏维生素A会引起坏血病 | |
| B. | 棉花、塑料、羊毛都属于天然有机高分子材料 | |
| C. | 食用的水产品可用甲醛水溶液浸泡、保鲜,市民可放心食用 | |
| D. | 香烟烟气中的一氧化碳是一种极易与血液中的血红蛋白结合的有毒气体 |
13.将空的矿泉水瓶从高原地区带到平原,瓶子变瘪,原因是瓶内气体( )


| A. | 分子体积变小 | B. | 分子质量变小 | C. | 分子间隔变小 | D. | 分子数目减少 |
14.关于饱和溶液的叙述正确的是( )
| A. | 饱和溶液一定是浓溶液 | |
| B. | 增加溶质可使不饱和溶液变为饱和溶液 | |
| C. | 饱和溶液就是不能再溶解任何物质的溶液 | |
| D. | 同一物质的饱和溶液一定比不饱和溶液的浓度大 |
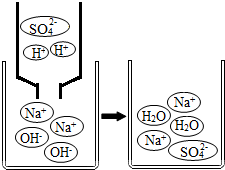 (1)向滴有酚酞试液的氢氧化钠溶液中逐滴滴入稀硫酸,溶液pH逐渐减小(填“增大”或“减小”).
(1)向滴有酚酞试液的氢氧化钠溶液中逐滴滴入稀硫酸,溶液pH逐渐减小(填“增大”或“减小”).