题目内容
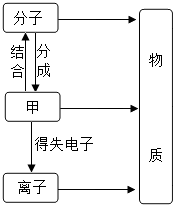 构成物质的粒子之间的关系如图所示:
构成物质的粒子之间的关系如图所示:(1)甲是
(2)在水,汞,氯化钠三物质中,由离子组成的物质是
(3)电解水实验可证明水的组成,其反应的化学方程式为
考点:分子、原子、离子、元素与物质之间的关系,电解水实验,根据化学反应方程式的计算
专题:有关化学方程式的计算,物质的微观构成与物质的宏观组成,空气与水
分析:(1)根据物质、分子、原子、离子之间的关系分析填空.构成物质的微粒有分子、原子、离子,分子是由原子构成的,原子通过得失电子形成离子;
(2)金属由原子直接构成,非金属氧化物由分子构成,盐类物质一般由离子构成;保持水的化学性质的最小粒子是水分子;
(3)根据电解水得到氢气和氧气都是气体可知,被电解的水质量是多少溶液质量就减少多少,根据硫酸钠质量不变计算出电解水完毕后剩余溶液质量,再根据溶液质量的减少量算出被电解水的质量.
(2)金属由原子直接构成,非金属氧化物由分子构成,盐类物质一般由离子构成;保持水的化学性质的最小粒子是水分子;
(3)根据电解水得到氢气和氧气都是气体可知,被电解的水质量是多少溶液质量就减少多少,根据硫酸钠质量不变计算出电解水完毕后剩余溶液质量,再根据溶液质量的减少量算出被电解水的质量.
解答:解:(1)构成物质的微粒有分子、原子、离子,分子是由原子构成的,原子通过得失电子形成离子.故答案为:原子;
(2)构成物质的微粒有分子、原子和离子,金属汞是由汞原子构成的,水是由水分子构成的,氯化钠是由钠离子和氯离子构成的.保持水的化学性质的最小粒子是水分子;
(3)水通电分解生成氢气和氧气,反应的化学方程式为2H2O
2H2↑+O2↑;硫酸钠在通电前后质量和性质不变,所以电解水完毕后溶液质量为:
=80g,溶液质量减少了:0.2克+99.8克-80克=20克.
答案:(1)原子;(2)氯化钠;水分子;(3)20.
(2)构成物质的微粒有分子、原子和离子,金属汞是由汞原子构成的,水是由水分子构成的,氯化钠是由钠离子和氯离子构成的.保持水的化学性质的最小粒子是水分子;
(3)水通电分解生成氢气和氧气,反应的化学方程式为2H2O
| ||
| 0.2g |
| 0.25% |
答案:(1)原子;(2)氯化钠;水分子;(3)20.
点评:本题主要考查了物质、分子、原子、离子之间的关系,认识物质的微粒性,能从微观上描述物质的构成.知道电解水实验的产物,及实验过程中的注意事项,加入氢氧化钠或是硫酸能够增强导电性,加速分解.能够根据实验现象结合质量守恒定律来书写化学方程式.

练习册系列答案
相关题目
已知两种分子 E 和 G 反应生成另外两种分子 L 和 M(如图).则下列判断正确的是( )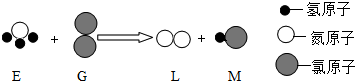
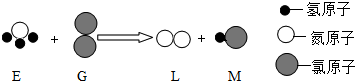
| A、G和M是单质 |
| B、L可能是化合物 |
| C、这是一种化合反应 |
| D、该反应体现了化学反应中原子不可再分 |
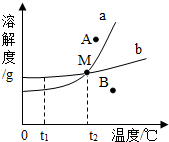
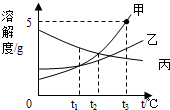 如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空: 端午节期间,邵阳地区大雨不断,资江河水猛涨,河水浑浊,水质受到一定程序污染,人们的生活用水必需经过一系列净化处理才能使用.
端午节期间,邵阳地区大雨不断,资江河水猛涨,河水浑浊,水质受到一定程序污染,人们的生活用水必需经过一系列净化处理才能使用.