题目内容
17. 实验室用过量的稀盐酸和大理石制取CO2,取100g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.
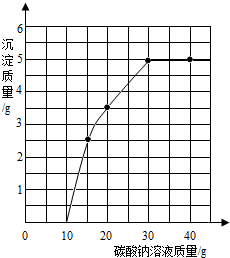
实验室用过量的稀盐酸和大理石制取CO2,取100g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.回答下列问题:
(1)从图中看出生成沉淀的最大质量是5g.
(2)计算碳酸钠溶液中溶质的质量分数.
(3)开始加入碳酸钠溶液至10g时,还没有沉淀的原因是碳酸钠先与过量的稀盐酸反应,当稀盐酸消耗完后,碳酸钠才与氯化钙反应生成碳酸钙沉淀.
分析 (1)根据图示信息找出沉淀的最大质量;
(2)根据氯化钙与碳酸钠反应的方程式,由沉淀的质量可求出碳酸钠的质量,再由溶质的质量分数计算;
(3)根据稀盐酸过量,故加入碳酸钠后首先与过量的稀盐酸反应,然后再与氯化钙反应进行解答.
解答 解:(1)由图示可以看出,生成沉淀的最大质量是5g;
(2)由图可以看出,与氯化钙反应的碳酸钠的质量是:30g-10g=20g
设20克碳酸钠溶液中碳酸钠的质量为x.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 5g
$\frac{106}{100}=\frac{x}{5g}$ 解得:x=5.3g
碳酸钠溶液中溶质的质量分数是:$\frac{5.3g}{20g}×100%$=26.5%
答:碳酸钠溶液中碳酸钠的质量分数为26.5%
(3)碳酸钠先与过量的稀盐酸反应,当稀盐酸消耗完后,碳酸钠才与氯化钙反应生成碳酸钙沉淀.
故答为:(1)5;(2)碳酸钠溶液中碳酸钠的质量分数为26.5%;(3)碳酸钠先与过量的稀盐酸反应,当稀盐酸消耗完后,碳酸钠才与氯化钙反应生成碳酸钙沉淀.
点评 此题是对物质分析及图象识别考查题,解题的关键是能对表格及图象有明确的认识,解决此题对培养学生良好的分析问题的能力有一定帮助.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
7.下列有关物质的用途主要由其物理性质决定的是( )
| A. | 氢气用作绿色能源 | B. | 氧气用于医疗急救 | ||
| C. | 铜丝用作电线 | D. | 酒精用于医疗消毒 |
8.某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为50%,将60g该混合物高温煅烧至固体质量不再改变,则生成二氧化碳的质量是( )
| A. | 16g | B. | 18g | C. | 20g | D. | 22g |
2.如图所示是几幅与化学有关的图片.下列对图中内容的分析正确的是( )
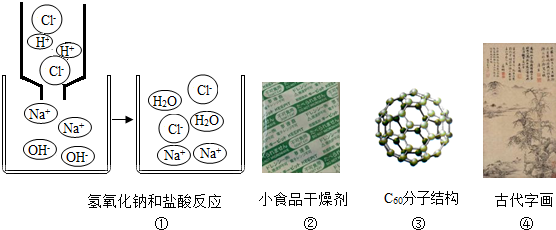

| A. | 图①可反映酸和碱发生中和反应的实质是:H++Cl-+Na++Cl-═NaCl+H2O | |
| B. | 图②中石灰干燥剂的干燥原理是:CaO+CO2═CaCO3 | |
| C. | 图③中的C60是由60个碳原子构成的 | |
| D. | 图④中古代字画能够保存很长时间不褪色的原因是常温下碳的化学性质稳定 |
9.“碳海绵”是已知的固体材料,只由碳元素组成,具有多孔结构,弹性好.它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状.下列关于碳海绵的说法中不正确的是( )
| A. | 具有吸附性 | B. | 可重复使用 | ||
| C. | 属于复合材料 | D. | 可处理海上泄露的石油 |
6.下列物质的名称、俗名与化学式完全对应的是( )
| A. | 氢氧化钙 熟石灰 CaO | B. | 汞 水银 Hg | ||
| C. | 葡萄糖 淀粉 C6H12O6 | D. | 碳酸钠 烧碱 Na2CO3 |
6.把X、Y、Z三种金属分别浸入相同质量分数的稀硫酸中,Y表面有气泡产生,X、Z表面无明显变化;把Z金属浸入X的硝酸盐溶液中,Z表面析出X.则三种金属的活动性顺序由强到弱的是( )
| A. | Y、Z、X | B. | X、Y、Z | C. | X、Z、Y | D. | Z、Y、X |
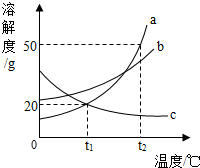 如图是a、b、c三种固体物质的溶解度曲线,请回答列问题.
如图是a、b、c三种固体物质的溶解度曲线,请回答列问题.