题目内容
15.某同学用食品脱氧剂(2g铁粉、0.5g活性炭、0.5g食盐)进行如下两个实验:实验Ⅰ:
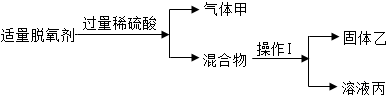
请回答:①操作Ⅰ的名称是过滤.
②溶液丙中含有的阳离子是Fe2+、Na+、H+(写微粒符号).
实验Ⅱ:将乙洗涤烘干后,二氧化碳通过灼热的乙生成丁.
进行如下实验,物质之间的转化关系如图(部分产物略去).
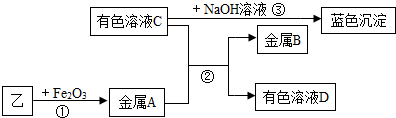
①金属A与B的活动性:A>B(填“>”“<”或“﹦”);
②区别有色溶液C与有色溶液D的方法是观察溶液颜色,蓝色为CuSO4溶液,浅绿色为FeSO4溶液;
③反应③的化学方程为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,不用填,
④向溶液C中加入BaCl2溶液,有白色沉淀产生.其化学方程式为CuSO4+BaCl2═BaSO4↓+CuCl2.
分析 实验Ⅰ:根据不溶于液体的固体和液体分离的一种方法,根据自制脱氧剂的成分的性质分析溶液丙中含有的阳离子;
实验Ⅱ:①根据金属A可以从溶液C中置换出金属B进行分析;
②根据溶液的颜色不同区别溶液C、D;
③根据硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠进行分析;
④根据氯化钡和硫酸铜反应生成硫酸钡沉淀和氯化铜进行分析.
解答 解:实验Ⅰ:不溶于液体的固体和液体分离的一种方法是过滤,所以操作a是过滤;由自制脱氧剂的成分可知,硫酸与铁反应生成了硫酸亚铁.所以,溶液丙中含有的溶质是硫酸亚铁、剩余的硫酸,和原混合物中的氯化钠,所以溶液丙中含有的阳离子是Fe2+、Na+、H+;
实验Ⅱ:①金属A可以从溶液C中置换出金属B,所以金属A与B的活动性:A>B;
②由上述分析可知,溶液C、D分别是硫酸铜和硫酸亚铁,由于颜色的不同.区别溶液C与溶液D物质的方法是观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液;
③硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
④氯化钡和硫酸铜反应生成硫酸钡沉淀和氯化铜,化学方程式为:CuSO4+BaCl2═BaSO4↓+CuCl2.
故答案为:实验Ⅰ:过滤;Fe2+、Na+、H+;
实验Ⅱ:①>;
②观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液;
③CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
④CuSO4+BaCl2═BaSO4↓+CuCl2.
点评 本题主要考查实验探究方面的知识,解答时要依据物质的性质分析反应流程图,明确具体的物质性质来解决相关问题.

练习册系列答案
相关题目
5.某一固体在试管中加热后,试管中没有固体残余物,有关该变化的说法正确的是( )
| A. | 一定是物理变化 | B. | 不能肯定是什么变化 | ||
| C. | 一定是化学变化 | D. | 既是物理变化又是化学变化 |
6.我们生活在物质的世界里,而物质在不断地变化.以下属于物理变化的是( )
| A. | 汽油燃烧 | B. | 牛奶发酸 | C. | 雕刻木器 | D. | 白菜腐烂 |
7.用化学用语填空
(1)3个氯原子3Cl;
(2)2个亚铁离子2Fe2+;
(3)天然气的主要成分CH4;
(4)写出高锰酸钾的化学式并标出其中锰元素的化合价K$\stackrel{+7}{Mn}$O4.
(1)3个氯原子3Cl;
(2)2个亚铁离子2Fe2+;
(3)天然气的主要成分CH4;
(4)写出高锰酸钾的化学式并标出其中锰元素的化合价K$\stackrel{+7}{Mn}$O4.
4.除去下列物质中混有的少量杂质(括号内为杂质),方法正确的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | CO2气体(CO) | 点燃 |
| B | N2气体(CO2) | 通过澄清石灰水 |
| C | K2CO3固体(KCl) | 加水溶解,过滤 |
| D | Na2NO3溶液(Na2SO4) | 加盐酸 |
| A. | A | B. | B | C. | C | D. | D |
20. 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:
【资料卡片】:
a、SiO2不溶于水、且不与酸反应,高温不分解;
b、NaHCO3受热易分解,生成Na2CO3、H2O、CO2;
c、牙膏中保湿剂、增稠剂、香精等均为有机物(有机物在高温加热条件下转化为气体).
(1)取一小段牙膏,加入蒸馏水,充分搅拌后静置,测得其上层清液的pH为8.3,则此牙膏显弱碱性,实验室能否用pH试纸测得该数值,请你作出判断并说明理由.不能,因为pH试纸只能测定出整数值;
(2)小岳同学发现,此品牌牙膏在冬季会出现颗粒变大的现象.资料显示是牙膏中的K12(一种钠盐)析出,则K12的溶解度和温度的关系是K12的溶解度随温度降低而降低;
(3)为测定此牙膏中SiO2的质量分数,兴趣小组同学设计了如下方案,并进行了3次实验:
【实验步骤】:
①准确称取2.0g牙膏膏体,烘干水分,高温加热,至质量不再减轻为止,在干燥器中冷却至室温;
②转移剩余物至烧杯中,加入稀HCl,至气体不再产生为止;
③过滤、洗涤、称量得到剩余固体质量(如表);
④根据实验数据进行计算.
【数据处理】:
(4)此测定做3次实验的目的是提高实验的精确度;
(5)综合上述实验方案及实验数据,计算此牙膏中SiO2的质量分数.22%;
【实验分析】:
(6)按上述实验步骤操作,发现测定结果偏大,导致偏大的原因可能是步骤③中,没有将剩余固体进行干燥,有洗涤液附着在固体表面;
(7)高温加热的目的除为了除去CaCO3及NaHCO3以外,还为除去保湿剂、增稠剂、香精等有机物;
(8)步骤②中,加稀HCl发生的反应有CaO+2HCl═CaCl2+H2O、Na2CO3+2HCl═2NaCl+H2O+CO2↑(用化学方程式表示);
(9)步骤③中,洗涤的目的是除去固体表面附着的CaCl2和NaCl溶液,若不洗涤,则测定结果将偏大(填“偏大”、“偏小”或“不变”);
(10)为保证洗涤效果,最好用A洗涤.
A.蒸馏水 B.自来水 C.饱和NaCl溶液 D.饱和CaCl2溶液.
 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:【资料卡片】:
a、SiO2不溶于水、且不与酸反应,高温不分解;
b、NaHCO3受热易分解,生成Na2CO3、H2O、CO2;
c、牙膏中保湿剂、增稠剂、香精等均为有机物(有机物在高温加热条件下转化为气体).
(1)取一小段牙膏,加入蒸馏水,充分搅拌后静置,测得其上层清液的pH为8.3,则此牙膏显弱碱性,实验室能否用pH试纸测得该数值,请你作出判断并说明理由.不能,因为pH试纸只能测定出整数值;
(2)小岳同学发现,此品牌牙膏在冬季会出现颗粒变大的现象.资料显示是牙膏中的K12(一种钠盐)析出,则K12的溶解度和温度的关系是K12的溶解度随温度降低而降低;
(3)为测定此牙膏中SiO2的质量分数,兴趣小组同学设计了如下方案,并进行了3次实验:
【实验步骤】:
①准确称取2.0g牙膏膏体,烘干水分,高温加热,至质量不再减轻为止,在干燥器中冷却至室温;
②转移剩余物至烧杯中,加入稀HCl,至气体不再产生为止;
③过滤、洗涤、称量得到剩余固体质量(如表);
| 实验编号 | 1 | 2 | 3 |
| 实验前(g) | 2.00 | 2.00 | 2.00 |
| 实验后(g) | 0.43 | 0.44 | 0.45 |
【数据处理】:
(4)此测定做3次实验的目的是提高实验的精确度;
(5)综合上述实验方案及实验数据,计算此牙膏中SiO2的质量分数.22%;
【实验分析】:
(6)按上述实验步骤操作,发现测定结果偏大,导致偏大的原因可能是步骤③中,没有将剩余固体进行干燥,有洗涤液附着在固体表面;
(7)高温加热的目的除为了除去CaCO3及NaHCO3以外,还为除去保湿剂、增稠剂、香精等有机物;
(8)步骤②中,加稀HCl发生的反应有CaO+2HCl═CaCl2+H2O、Na2CO3+2HCl═2NaCl+H2O+CO2↑(用化学方程式表示);
(9)步骤③中,洗涤的目的是除去固体表面附着的CaCl2和NaCl溶液,若不洗涤,则测定结果将偏大(填“偏大”、“偏小”或“不变”);
(10)为保证洗涤效果,最好用A洗涤.
A.蒸馏水 B.自来水 C.饱和NaCl溶液 D.饱和CaCl2溶液.