题目内容
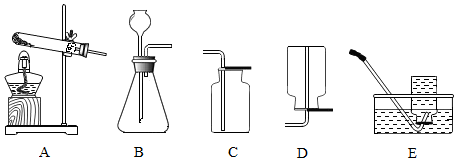
8.为保证木炭、硫粉和铁丝燃烧实验的顺利演示,教师准备用125mL的集气瓶收集8瓶氧气.(1)硫粉在氧气中燃烧的现象是发出蓝紫色火焰,产生有刺激性气味的气体,放热.
(2)铁丝在氧气中燃烧的化学方程式是3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;反应类型化合反应.
(3)用高锰酸钾制氧气的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;反应类型分解反应.反应中,高锰酸钾和氧气的质量比是79:8.
分析 (1)根据硫粉燃烧现象回答;
(2)根据铁丝在氧气中燃烧生成了四氧化三铁写出反应的化学方程式,根据反应的特点分析反应的类型;
(3)根据用高锰酸钾制氧气的原子写出反应的化学方程式,根据反应的特点分析反应的类型;根据方程式计算出的高锰酸钾和氧气的质量比.
解答 解:(1)硫粉在氧气中燃烧:发出蓝紫色火焰,产生有刺激性气味的气体,放热;
(2)铁丝在氧气中燃烧生成四氧化三铁,反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,该反应由两种物质生成了一种物质,属于化合反应;
(3)用高锰酸钾制氧的反应物为高锰酸钾,反应条件为加热,生成物为锰酸钾、二氧化锰、氧气,则反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应符合“一分多”的特点,属于分解反应;
反应中高锰酸钾和氧气的质量比为:[2×(39+55+64)]:32═79:8
故答案为:(1)发出蓝紫色火焰,产生有刺激性气味的气体,放热;(2)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,化合反应;(3)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,分解反应; 79:8.
点评 本题考查了化学方程式的书写和计算的有关知识,考查较为全面.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
14.下列有关溶液的说法,正确的是( )
| A. | 溶液一定是混合物 | B. | 溶剂一定是水 | ||
| C. | 溶质一定是固体 | D. | 溶液一定是无色透明的 |
15.造成酸雨的主要物质是( )
| A. | 一氧化碳和二氧化碳 | B. | 二氧化硫和二氧化氮 | ||
| C. | 甲烷和一氧化碳 | D. | 二氧化硫和一氧化碳 |
3.钾肥能促进作物茎秆粗壮,增强对病虫害和倒伏的抵抗能力.下列物质中不能用作钾肥的是( )
| A. | 氯化钾 | B. | 氢氧化钾 | C. | 碳酸钾 | D. | 硫酸钾 |
13.如表是活禽市场某种消毒液的主要成分:
请根据此表,将下列带点部分的内容用恰当的化学用语填写在横线上:
(1)该消毒液的溶剂H2O;
(2)该消毒液中含有的金属离子Ag+;
(3)标注硝酸中氮元素的化合价H$\stackrel{+5}{N}$O3.
| 用 途 | 杀菌消毒 |
| 主要成分 | 硝酸、硝酸银、过氧化氢 |
(1)该消毒液的溶剂H2O;
(2)该消毒液中含有的金属离子Ag+;
(3)标注硝酸中氮元素的化合价H$\stackrel{+5}{N}$O3.
18.下列属于化学性质的是( )
| A. | 延展性 | B. | 腐蚀性 | C. | 吸附性 | D. | 挥发性 |