题目内容
小明同学往氢氧化钙溶液中滴加稀盐酸,没有滴加酸碱指示剂.为了确认滴加的盐酸是否已经过量.从烧杯中取少量反应后的溶液于试管中,用某种试剂进行检验.如表是小明同学设计的实验方案,其中不正确的是 ( )
| 实验方案 | 使用试剂 | 判断方法 |
| ① | 石灰石 | 如果有气泡产生,表明盐酸已经过量 |
| ② | pH试纸 | 如果pH<7,表明盐酸已经过量 |
| ③ | 金属铜 | 如果有气泡产生,表明盐酸已经过量 |
| ④ | 紫色石蕊试液 | 如果溶液变成红色,表明盐酸已经过量 |
| A、A | B、B | C、C | D、D |
考点:中和反应及其应用,酸的化学性质,溶液的酸碱性与pH值的关系
专题:常见的酸 酸的通性
分析:A、根据盐酸会与碳酸钙反应生成气体进行分析,
B、根据PH值确定溶液的酸碱性进行分析,
C、根据氯离子会与银离子生成沉淀进行分析,
D、根据酸会使紫色石蕊变色进行分析.
B、根据PH值确定溶液的酸碱性进行分析,
C、根据氯离子会与银离子生成沉淀进行分析,
D、根据酸会使紫色石蕊变色进行分析.
解答:解:A、碳酸钙会与盐酸反应生成二氧化碳气体,只要有气泡产生,说明酸过量了,故A正确,
B、PH试纸测出的PH值小于7,说明溶液显酸性,盐酸就过量了,故B正确,
C、铜在金属活动性顺序中排在H的后面,不能和酸反应,故C不正确,
D、紫色石蕊变红色,说明溶液中存在氢离子,也就可以证明盐酸过量,故D正确.
故选C.
B、PH试纸测出的PH值小于7,说明溶液显酸性,盐酸就过量了,故B正确,
C、铜在金属活动性顺序中排在H的后面,不能和酸反应,故C不正确,
D、紫色石蕊变红色,说明溶液中存在氢离子,也就可以证明盐酸过量,故D正确.
故选C.
点评:在解此类题时,首先分析需要验证的物质的化学性质,然后选择适当的试剂,出现不同的现象即可鉴别.

练习册系列答案
相关题目
为了改善保定市空气质量,我市部分公交车已改为压缩天然气(CNG)为动力燃料.天然气中含有甲烷和其它一些物质,天然气属于( )
| A、混合物 | B、化合物 |
| C、氧化物 | D、单质 |
电影《黄金大劫案》上映后,里面用“王水”(浓盐酸与浓硝酸的混合液)溶解黄金的情引起了广泛的热议.“王水”溶解黄金的化学方程式为:Au+HNO3+xHCl═HAuCl4+NO↑+2H2O,其中x的数值和四氯合金酸(HAuCl4)中金元素的化合价分别是( )
| A、2,+7价 |
| B、4,+3价 |
| C、4,+7价 |
| D、4,-7价 |
下列所描述的现象,从化学的角度理解不正确的是( )
| A、花香四溢:分子在不断运动 |
| B、热胀冷缩:分子的大小发生了变化 |
| C、干冰升华:分子本身没有发生变化 |
| D、火要空心:增加可燃物与空气的接触面积 |
下列实验基本操作正确的是( )
A、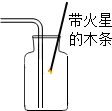 氧气验满 |
B、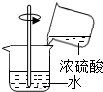 稀释浓硫酸 |
C、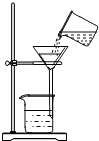 过滤 |
D、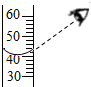 读取液体体积 |
R为金属,发生如下反应:R+CuSO4═Cu+RSO4,下列说法错误的是( )
| A、该反应为置换反应 |
| B、R的金属活动性比Cu强 |
| C、该金属为Al |
| D、若R为Fe,反应后溶液的质量会减小 |
在化合、分解、置换、复分解四类基本反应类型中,可能生成水的反应共有( )
| A、一类 | B、二类 | C、三类 | D、四类 |
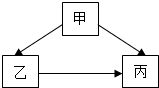 甲、乙、丙是初中化学常见的物质,其转化关系如图所示:
甲、乙、丙是初中化学常见的物质,其转化关系如图所示: