题目内容
1.(1)实验现象:与电源正极相连的一端产生气体体积少,与负极相连的一端产生气体是氢气,负、正极产生的气体体积比约为2:1(2)气体检验:用带火星的木条检验乙管中的气体,发现木条复燃,说明是氧气.用燃着的木条检验甲管中的气体,能燃烧,火焰呈蓝色,是氢气.
分析 1)根据电解水的实验现象、结论及生成气体的性质回答.电解水负极生成氢气和正极氧气的体积比是2:1;
(2)根据氢气具有可燃性,氧气能支持燃烧解答.
解答 解:(1)电解水时两极上都出现气泡,与电源正极相连的一端产生气体体积少,与负极相连的一端产生气体是氢气;正负两极产生的气体的体积比是1:2;
(2)在电解水的实验中,必须用燃着的木条来检验的是由负极产生的气体,检查时出现的现象是:气体能燃烧产生淡蓝色的火焰,可以用带火星木条检验的是由正极产生的气体,检验时产生的现象是能使用带火星的木条复燃.
故答案为:(1)氢气、2:1;(2)带火星的木条、燃着的木条、蓝色.
点评 熟记电解水实验中的现象,分清氢气和氧气的质量比和体积比,这点很重要.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
16.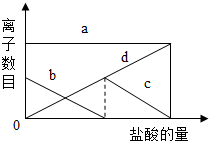 向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.(提示:先后发生的反应为:
向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.(提示:先后发生的反应为:
①K2CO3+HCl═KHCO3+KCl,②KHCO3+HCl═KCl+H2O+CO2↑).
如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是
( )
 向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.(提示:先后发生的反应为:
向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡.随着盐酸的加入,溶液中离子数目也相应地发生变化.(提示:先后发生的反应为:①K2CO3+HCl═KHCO3+KCl,②KHCO3+HCl═KCl+H2O+CO2↑).
如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是
( )
| A. | a:K+; b:CO32-; c:HCO3-; d:Cl- | |
| B. | a:K+; b:CO32-; c:Cl-; d:HCO3- | |
| C. | a:Cl-; b:K+; c:CO32-; d:HCO3- | |
| D. | a:K+; b:HCO3-; c:Cl-; d:CO32- |
6.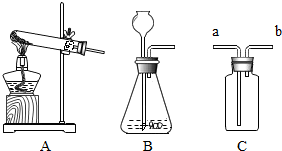 科学兴趣小组学习了二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
科学兴趣小组学习了二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
(一)选择装置并检查气密性.
(二)称取0.1克的二氧化锰粉末加入容器中.
(三)量取50毫升溶质质量分数约1%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积.
(四)改变二氧化锰的质量,重复上述实验,记录数据如表.
(1)本实验探究的问题是二氧化锰的质量对过氧化氢分解快慢的影响.
(2)实验中除了量筒外,还需要用到的测量仪器有天平、或秒表.
(3)为完成本实验,应选择如图气体发生和收集装置中的组合是BC.做完“铁在氧气里燃烧”实验后,小冬同学有两个疑惑不解的问题,于是她进行了以下探究活动,请你一同参与.
[问题1]铁燃烧时溅落下来的黑色物质中还有没有铁呢?
[查阅资料1]自然界中铁的氧化物主要是Fe3O4(黑色)和Fe2O3(红棕色)两种(FeO极易被氧化为Fe2O3);铁的氧化物均能溶于酸的溶液不产生气体,而铁能溶于酸的溶液但会放出气体.
[实验探究]:将冷却后的黑色物质碾碎,装入试管,加入盐酸中,观察到的现象是冒气泡(或生成红色固体),说明铁燃烧时溅落下来的黑色物质中还含有铁.
[问题2]铁燃烧的产物为什么不是Fe2O3呢?
[查阅资料2]:(1)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
(1)Fe2O3高温时分解成Fe3O4.
[理论探讨]:根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在l535℃~l538℃之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
[拓展延伸]:有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色由黑色变成红棕色,就说明包装盒破损进气,这样售货员就能及时发现并处理.写出该反应的化学方程式FeO+O2=Fe2O3.
 科学兴趣小组学习了二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
科学兴趣小组学习了二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.(一)选择装置并检查气密性.
(二)称取0.1克的二氧化锰粉末加入容器中.
(三)量取50毫升溶质质量分数约1%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积.
(四)改变二氧化锰的质量,重复上述实验,记录数据如表.
| 时间/秒 | 生成氧气的体积/毫升 | |||
| 0.1克MnO2 | 0.2克MnO2 | 0.3克MnO2 | 0.4克MnO2 | |
| 40 | 49 | 61 | 75 | 86 |
| 80 | 77 | 87 | 90 | 92 |
| 120 | 89 | 92 | 92 | 92 |
| 160 | 92 | 92 | 92 | 92 |
(2)实验中除了量筒外,还需要用到的测量仪器有天平、或秒表.
(3)为完成本实验,应选择如图气体发生和收集装置中的组合是BC.做完“铁在氧气里燃烧”实验后,小冬同学有两个疑惑不解的问题,于是她进行了以下探究活动,请你一同参与.
[问题1]铁燃烧时溅落下来的黑色物质中还有没有铁呢?
[查阅资料1]自然界中铁的氧化物主要是Fe3O4(黑色)和Fe2O3(红棕色)两种(FeO极易被氧化为Fe2O3);铁的氧化物均能溶于酸的溶液不产生气体,而铁能溶于酸的溶液但会放出气体.
[实验探究]:将冷却后的黑色物质碾碎,装入试管,加入盐酸中,观察到的现象是冒气泡(或生成红色固体),说明铁燃烧时溅落下来的黑色物质中还含有铁.
[问题2]铁燃烧的产物为什么不是Fe2O3呢?
[查阅资料2]:(1)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
[理论探讨]:根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在l535℃~l538℃之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
[拓展延伸]:有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色由黑色变成红棕色,就说明包装盒破损进气,这样售货员就能及时发现并处理.写出该反应的化学方程式FeO+O2=Fe2O3.
10.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,同学们产生了疑问:反应后的溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四或四.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,则甲组猜想中的NaOH或氢氧化钠不正确.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师指出【实验探究】(2)中存在两处明显错误,只有一个方案和操作都正确,请
大家反思后,写出该方案中反应的化学方程式:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,同学们产生了疑问:反应后的溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四或四.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,则甲组猜想中的NaOH或氢氧化钠不正确.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaC12溶液 |
| 实验操作 |  | 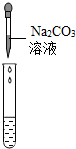 | 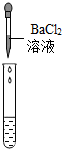 |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 产生无色气泡有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师指出【实验探究】(2)中存在两处明显错误,只有一个方案和操作都正确,请
大家反思后,写出该方案中反应的化学方程式:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.
 如图中A-F分别表示一种常见化合物,A、B都是氧化物,A通常为气态,F常用于实验室制取A(部分生成物已略去).
如图中A-F分别表示一种常见化合物,A、B都是氧化物,A通常为气态,F常用于实验室制取A(部分生成物已略去).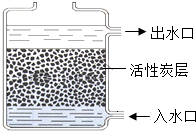 水是生命之源,没有水就没有生命.
水是生命之源,没有水就没有生命.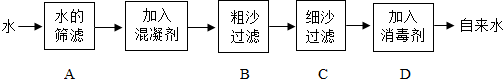
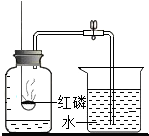 下面是测定空气中氧气体积分数的实验.在集气瓶内预先装少量水,余下的容积5等分,做好标记,在带橡皮塞和导管的燃烧匙内装足量的红磷,用弹簧夹夹紧乳胶管,点燃燃烧匙内的红磷,立即伸入集气瓶内,塞紧橡皮塞(如图).待红磷熄灭并冷却到室温后,打开弹簧夹.
下面是测定空气中氧气体积分数的实验.在集气瓶内预先装少量水,余下的容积5等分,做好标记,在带橡皮塞和导管的燃烧匙内装足量的红磷,用弹簧夹夹紧乳胶管,点燃燃烧匙内的红磷,立即伸入集气瓶内,塞紧橡皮塞(如图).待红磷熄灭并冷却到室温后,打开弹簧夹.