题目内容
为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出)。产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算:
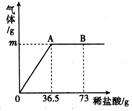
⑴A点产生气体的质量为 ;
⑵试样中碳酸钠的质量分数(结果精确到0.1%);
⑶B点时,烧杯内溶液中溶质的化学式 。
(1)2.2g
(2)解:设6g试样中Na2CO3质量为x
Na2CO3 + 2HCl = 2Na Cl + H2O + CO2↑
Cl + H2O + CO2↑
106 44
X 2.2g
106 : 44 = x : 2.2g
X = 5.3g
试样中Na2CO3的质量分数为:
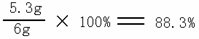
答:试样中Na2CO3的质量分数为88.3%
(3)NaCl、HCl
解析:根据题意产生的气体的质量是反应前的质量和减去反应后溶液的质量,根据二氧化碳的质量可以求出碳酸钠的质量,溶液中的溶质既有生成物氯化钠还有未反应完的氯化氢两种溶质。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 ;
; ”、“无影响”),原因是 。反应方程式为
”、“无影响”),原因是 。反应方程式为