题目内容
6.现有两瓶失去标签的溶液,溶质分别可能是硝酸钠、硝酸铜、硫酸钠、硫酸、碳酸钾中的一种,检验步骤如下:Ⅰ.分别取少量混用,无明显现象,溶液无色透明,经测定混合溶液显酸性.由此可推断这两瓶溶液中的溶质一定不是Cu(NO3)2、K2CO3;(填化学式,多填、少填、错填均不得分,下同)
Ⅱ.向上述混合溶液中加入Ba(NO3)2溶液,产生白色沉淀.则这两瓶溶液的溶质至少是H2SO4、Na2SO4中的一种;反应的化学方程式为Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 (任意一个即可);
试推断这两瓶溶液的溶质可能的组合有4种(填数字),请写出其中含阳离子种类最少的一种组合Na2SO4、NaNO3.
分析 根据硝酸铜在溶液中显蓝色,稀硫酸显酸性,碳酸钾溶液显碱性硫酸钠、硝酸钠溶液显中性等知识进行分析.
解答 解:硝酸铜在溶液中显蓝色,稀硫酸显酸性,碳酸钾溶液显碱性硫酸钠、硝酸钠溶液显中性.
Ⅰ、分别取少量混用,无明显现象,溶液无色透明,经测定混合溶液显酸性.由此可推断这两瓶溶液中的溶质一定不是:Cu(NO3)2、K2CO3;
Ⅱ.向上述混合溶液中加入Ba(NO3)2溶液,产生白色沉淀.则这两瓶溶液的溶质至少是H2SO4、Na2SO4中的一种;化学方程式为:Ba(NO3)2+H2SO4=BaSO4↓+2HNO3;
推断这两瓶溶液的溶质可能的组合有硝酸钠、硫酸钠,硝酸钠、硫酸,硫酸钠、硫酸,硝酸钠、硫酸、硫酸钠4种,请写出其中含阳离子种类最少的一种组合Na2SO4、NaNO3.
故答案为:Ⅰ、Cu(NO3)2、K2CO3;
Ⅱ.H2SO4、Na2SO4,Ba(NO3)2+H2SO4=BaSO4↓+2HNO3;
4,Na2SO4、NaNO3.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.下列说法不正确的是( )
| A. | 一氧化碳能用于炼铁--作燃料 | |
| B. | 氧气能支持燃烧--做助燃剂 | |
| C. | 石墨很软--润滑剂 | |
| D. | 小苏打能与盐酸反应--治疗胃酸过多 |
14.下列变化中发生化学变化的是( )
| A. | 干冰熔化 | B. | 石蜡熔化 | C. | 粮食酿酒 | D. | 空气液化 |
1.如图是甲、乙两物质的溶解度曲线(不含结晶水),下列说法正确的是( )


| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 乙的不饱和溶液降温可变为饱和溶液 | |
| C. | 20℃,甲乙两物质的溶解度相等 | |
| D. | 50℃,甲的饱和溶液溶质质量分数为40% |
15.下列关于金属材料的说法中,不正确的是( )
| A. | 生铁、钢都属于合金 | |
| B. | 铜有良好的导电性,可用于制作电线 | |
| C. | 铝锅要经常用钢丝球擦洗,防止生锈 | |
| D. | 地球上的金属资源大多以化合物的形式存在 |
16.可乐是一种常见的碳酸饮料,近日,一段“可乐灭火”的视频在网上流传,视频中,消防员手持一瓶可乐,拧开瓶盖,捂住瓶口使劲摇晃后将喷溅而出的可乐泡沫对准火焰进行喷射,很快火就被扑灭,下列对可乐及“可乐灭火”分析错误的是( )
| A. | “可乐泡沫”使可燃物隔绝了氧气 | |
| B. | 可乐能“喷溅而出”是由于压强改变所致 | |
| C. | 可乐瓶中如果装水也能产生“可乐灭火”的效果 | |
| D. | 消防员“使劲摇晃”的目的是为了加快二氧化碳逸出 |
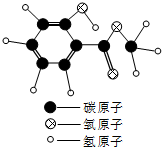 复方冬青软膏具有强力迅速镇痛作用,其有效成分A的分子模型如图所示.
复方冬青软膏具有强力迅速镇痛作用,其有效成分A的分子模型如图所示.