题目内容
10.三位同学分别用相同质量分数的稀盐酸,测定某石灰石样品中碳酸钙的质量分数(石灰石中的杂质既不与酸反应,也不溶于水).(1)小吴同学的方法可用如下图流程表示,测得的碳酸钙的质量分数为68%;他在过滤操作中,需要用到的玻璃仪器有C(选填序号).
A.酒精灯、漏斗、玻璃棒 B.长颈漏斗、试管、导管 C.漏斗、玻璃棒、烧杯

(2)小永同学取10g样品,用如下图甲实验装置进行实验,反应结束后,测得B装置质量增加了4.6克,算得碳酸钙的质量分数,发现与事实严重不符,造成这种情况的可能原因是:B装置吸收的气体中除了二氧化碳,还有大量水蒸气和氯化氢气体.
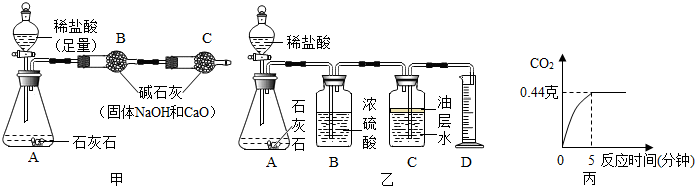
(3)小彬同学用如上图乙的实验装置进行实验,将20克稀盐酸加入到1.4克样品中,经折算,得到的CO2质量与反应时间的关系如图丙,求该石灰石样品中CaCO3的质量分数.
分析 (1)根据实验过程中的数据可以计算碳酸钙的质量分数;
在过滤操作中,需要用到的玻璃仪器有漏斗、玻璃棒、烧杯;
(2)盐酸易挥发;
碱石灰能够吸收水蒸气、二氧化碳和氯化氢气体;
(3)由图中信息可知生成二氧化碳的质量,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据反应的化学方程式和提供的数据可以计算碳酸钙的质量分数.
解答 解:(1)由反应过程可知,10g样品中含有3.2g杂质,因此样品中碳酸钙的质量分数为:$\frac{10g-3.2g}{10g}$×100%=68%,
在过滤操作中,需要用到的玻璃仪器有漏斗、玻璃棒、烧杯.
故填:68%;C.
(2)造成这种情况的可能原因是:B装置中的碱石灰吸收了二氧化碳、水蒸气和挥发出的氯化氢气体,导致测定结果不准确.
故填:B装置吸收的气体中除了二氧化碳,还有大量水蒸气和氯化氢气体.
(3)设样品中碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+CO2↑+H2O,
100 44
x 0.44g
$\frac{100}{x}$=$\frac{44}{0.44g}$,
x=1g,
碳酸钙质量分数为:$\frac{1g}{1.4g}$×100%=71.4%,
答:该样品中碳酸钙的质量分数为71.4%.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
18.实验操作有误或不规范,很可能造成实验失败或酿成事故.下列实验基本操作中正确的是( )
| A. |  闻气体气味 | B. | 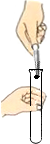 取用块状固体 | C. | 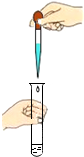 滴加液体 | D. | 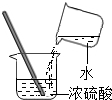 稀释浓硫酸 |
5.少量的激活剂或抑制剂就会影响酶的活性,有些离子是酶的激活剂(即增强酶的活性),有些离子则是酶的抑制剂(即减弱酶的活性),某研究小组为探究唾液淀粉酶的激活剂和抑制剂,设计如下实验:
实验材料:唾液淀粉酶、3%淀粉溶液、碘液、0.3%NaCl溶液、1%CuSO4溶液、1%Na2SO4溶液、蒸馏水.
实验设置:
注:实验中加入缓冲液的作用是维持反应液中pH的稳定.
实验结果,多次取样,用碘液进行鉴定,记录每次取样溶液的颜色情况(见下表,“+”表示蓝色程度;蓝色变到黄色的过程,表示淀粉最后被完全分解.)
请回答下列问题:
(1)该实验中设置1号试管的目的是对比作用;设置3号试管的目的是排除Na+,SO42-对酶活性的影响.
(2)分析实验结果可知:对酶活性有促进作用的离子是Cl-.
实验材料:唾液淀粉酶、3%淀粉溶液、碘液、0.3%NaCl溶液、1%CuSO4溶液、1%Na2SO4溶液、蒸馏水.
实验设置:
| 1组 | 2组 | 3组 | 4组 | |
| 3%淀粉溶液 | 2mL | 2mL | 2mL | 2mL |
| 唾液淀粉酶溶液 | 1mL | 1mL | 1mL | 1mL |
| pH6.8缓冲液 | 1mL | 1mL | 1mL | 1mL |
| 蒸馏水 | 1mL | |||
| 1%CuSO4溶液 | 1mL | |||
| 1%Na2SO4溶液 | 1mL | |||
| 0.3%NaCl溶液 | 1mL |
实验结果,多次取样,用碘液进行鉴定,记录每次取样溶液的颜色情况(见下表,“+”表示蓝色程度;蓝色变到黄色的过程,表示淀粉最后被完全分解.)
| 时间 | 试管号(对应相应的组号) | |||
| 1号 | 2号 | 3号 | 4号 | |
| 0.5min | 蓝++ | 蓝+++ | 蓝++ | 蓝++ |
| 1min | 蓝+ | 蓝+++ | 蓝+ | 紫 |
| 2min | 紫 | 蓝+++ | 紫 | 红棕色 |
| 3min | 红棕色 | 蓝+++ | 红棕色 | 棕黄色 |
| 4min | 棕黄色 | 蓝+++ | 棕黄色 | 黄色 |
| 5min | 黄色 | 蓝+++ | 黄色 | 黄色 |
| … | ||||
| 1h | ||||
(1)该实验中设置1号试管的目的是对比作用;设置3号试管的目的是排除Na+,SO42-对酶活性的影响.
(2)分析实验结果可知:对酶活性有促进作用的离子是Cl-.
15.证据是科学探究中获得结论的最重要的依据.让我们一起经历一次寻找证据的旅程吧.
【实验目的】制取纯净的硫酸钡
【反应原理】Na2SO4+BaCl2═BaSO4↓+2NaCl
【实验步骤】取一定量的硫酸钠和氯化钡溶液反应,过滤、洗涤、干燥得到纯净的硫酸钡.
(1)实验中,能直接观察到说明硫酸钠和氯化钡溶液发生化学反应的证据是:有白色沉淀生成.
(2)判断任一反应物是否完全反应的证据可按如下方法获取:
【实验目的】制取纯净的硫酸钡
【反应原理】Na2SO4+BaCl2═BaSO4↓+2NaCl
【实验步骤】取一定量的硫酸钠和氯化钡溶液反应,过滤、洗涤、干燥得到纯净的硫酸钡.
(1)实验中,能直接观察到说明硫酸钠和氯化钡溶液发生化学反应的证据是:有白色沉淀生成.
(2)判断任一反应物是否完全反应的证据可按如下方法获取:
| 猜想 | 方案 | 证据 | 结论 |
| 氯化钡可能已 完全反应 | 取少量滤液,加入稀硫酸 溶液,观察现象 | 无白色沉淀生成 | 氯化钡已完全反应 |
| 硫酸钠可能已 完全反应 | 取少量滤液,加入氯化钡溶液,观察现象 | 无白色沉淀生成 | 硫酸钠未完全反应 |
19. 2016年1月6日,朝鲜宣布第一枚氢弹成功试验,引起国际社会的关注.引爆氢弹极为困难,引爆需要在氢弹内部安放小型原子弹,瞬间达到反应条件温度,而原子弹中含铀元素(部分信息如图所示).下列有关铀说法错误的是( )
2016年1月6日,朝鲜宣布第一枚氢弹成功试验,引起国际社会的关注.引爆氢弹极为困难,引爆需要在氢弹内部安放小型原子弹,瞬间达到反应条件温度,而原子弹中含铀元素(部分信息如图所示).下列有关铀说法错误的是( )
 2016年1月6日,朝鲜宣布第一枚氢弹成功试验,引起国际社会的关注.引爆氢弹极为困难,引爆需要在氢弹内部安放小型原子弹,瞬间达到反应条件温度,而原子弹中含铀元素(部分信息如图所示).下列有关铀说法错误的是( )
2016年1月6日,朝鲜宣布第一枚氢弹成功试验,引起国际社会的关注.引爆氢弹极为困难,引爆需要在氢弹内部安放小型原子弹,瞬间达到反应条件温度,而原子弹中含铀元素(部分信息如图所示).下列有关铀说法错误的是( )| A. | 属于金属元素 | B. | 相对原子质量为238.0g | ||
| C. | 原子的核电荷数是92 | D. | 该元素的核外电子数为92 |
20.如图为甲、乙、丙三种物质的溶解度曲线.下列说法正确的是( )
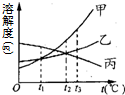

| A. | 在t1℃时,溶解度甲=乙<丙 | |
| B. | 从乙饱和溶液中析出较多量的晶体通常可采用降温结晶法 | |
| C. | 等质量的甲、乙饱和溶液从t3℃降温到t1℃,析出晶体(无结晶水)的质量甲>乙 | |
| D. | t2℃时,将乙、丙的饱和溶液升温至t3℃,乙溶液的溶质质量分数增大,丙溶液的溶质质量分数减小 |