题目内容
元素周期表是学习和研究化学的重要工具.下表是1-3周期元素的部分信息:

请认真分析表中信息,回答下列问题.
(1)核电荷数为7的元素属于 (填“金属元素”或“非金属元素”).
(2)第二周期共有8种元素,该周期元素原子的核外 数相同.
(3)3号元素和11号元素的化学性质相似的原因是它们的 数相同.
(4)写出Z元素原子结构示意图: ,制造太阳能汽车所用的太阳能电池需要大量的单质Z,单质Z是由石英固体(ZO2)与相对原子质量为12.01的元素在高温条件下反应制得的,同时生成一种可燃性气体,该反应的化学方程式为 .

请认真分析表中信息,回答下列问题.
(1)核电荷数为7的元素属于
(2)第二周期共有8种元素,该周期元素原子的核外
(3)3号元素和11号元素的化学性质相似的原因是它们的
(4)写出Z元素原子结构示意图:
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:(1)距核最远的称为最外层,最外层上电子数大于等于4为非金属元素,易得电子形成8电子稳定结构;
(2)根据元素周期表中同一周期的规定来分析;
(3)根据最外层电子数与化学性质的关系以及最外层电子数与化合价的关系来解答;
(4)根据元素周期表排列依据及原子结构示意图各部分含义分析;根据质量守恒定律写出化学方程式.
(2)根据元素周期表中同一周期的规定来分析;
(3)根据最外层电子数与化学性质的关系以及最外层电子数与化合价的关系来解答;
(4)根据元素周期表排列依据及原子结构示意图各部分含义分析;根据质量守恒定律写出化学方程式.
解答:解:
(1)最外层电子数为7,大于4,该元素为非金属元素;
(2)第二周期的3-10号元素原子的电子层数相同,第三周期的11-18号元素原子的电子层数也相同,因此得出规律每一周期元素原子的电子层数相同;
(3)3号和11号元素最外层电子数相同,都为1,在化学反应中都易失去一个电子达到稳定结构;
(4)元素周期表是按照原子序数递增顺序排列的,因此X的质子数14,原子结构示意图为: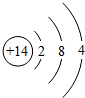
石英固体(ZO2)与相对原子质量为12.01的元素在高温条件下反应制得的,同时生成一种可燃性气体,该反应的化学方程式为:2C+SiO2
2CO+Si;
答案:
(1)非金属元素
(2)电子层
(3)最外层电子
(4)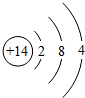 2C+SiO2
2C+SiO2
2CO+Si
(1)最外层电子数为7,大于4,该元素为非金属元素;
(2)第二周期的3-10号元素原子的电子层数相同,第三周期的11-18号元素原子的电子层数也相同,因此得出规律每一周期元素原子的电子层数相同;
(3)3号和11号元素最外层电子数相同,都为1,在化学反应中都易失去一个电子达到稳定结构;
(4)元素周期表是按照原子序数递增顺序排列的,因此X的质子数14,原子结构示意图为:
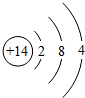
石英固体(ZO2)与相对原子质量为12.01的元素在高温条件下反应制得的,同时生成一种可燃性气体,该反应的化学方程式为:2C+SiO2
| ||
答案:
(1)非金属元素
(2)电子层
(3)最外层电子
(4)
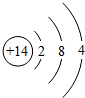 2C+SiO2
2C+SiO2
| ||
点评:了解元素周期表的特点及其应用;掌握原子原子得失电子的判断方法;掌握物质化学式的书写方法,本题难度不大.

练习册系列答案
相关题目
该药方涉及的化学反应原理为Ca(OH)2+K2CO3═CaCO3↓+2X,X是起到“食肉”作用的主要物质,其化学式为( )
| A、KH |
| B、H2O |
| C、K2O |
| D、KOH |
下列物质由分子构成的是( )
| A、钢 | B、氢气 | C、氯化钠 | D、硫酸锌 |
某学生测定的下列数据中,合理的是( )
| A、用10mL量筒量取了7.55mL水 |
| B、用pH试纸测得某地雨水的pH值为5.6 |
| C、测得某粗盐中氯化钠的质量分数为90.5% |
| D、用托盘天平称取16.70g的固体锌 |