题目内容
1.常温下,将20.0g质量分数为14.0%的KNO3溶液与30.0g质量分数为24.0%的KNO3溶液混合,得到密度为1.15g•cm-3的混合溶液.计算:(1)混合后溶液的质量分数.
(2)混合后溶液的物质的量浓度.
分析 (1)根据溶质质量分数的计算公式计算;
(2)根据硝酸钾的质量求出物质的量,再根据体积求出混合后溶液的物质的量浓度.
解答 解:(1)20.0g×14.0%+30.0g×24.0%=10.0 g,
溶液总质量为:20.0g+30.0g=50.0 g,
混合后溶液中KNO3的质量分数为:=$\frac{10.0g}{50.0g}$×100%=20%.
(2)混合后溶液中的KNO3的物质的量为:
n(KNO3)=$\frac{10g}{101g/mol}$≈0.099 mol,
混合后溶液的总体积为:V(KNO3)=$\frac{20.0g+30.0g}{1.15g/c{m}^{3}}$≈43.5cm3=0.0435L,
混合后溶液中KNO3的物质的量浓度为:
c(KNO3)=$\frac{0.099mol}{0.0435L}$≈2.28 mol/L.
答:(1)混合后溶液的质量分数是20%.
(2)混合后溶液的物质的量浓度是2.28 mol/L.
点评 本题属于有关溶液的简单计算,熟记计算的公式即可分析计算,在计算时应注意计算数据的准确性,

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.下列物质中属于电解质的是( )
| A. | 硝酸钾 | B. | 蔗糖 | C. | 金属铜 | D. | 食盐水 |
6.下列操作或现象与分子对应的特征一致的是B
| 选项 | 操作或现象 | 分子的特征 |
| A | 100ml酒精和100ml水混在一起,体积小于200ml | 分子是有质量的 |
| B | 在花园中能闻到花的香味 | 分子是运动的 |
| C | 热胀冷缩 | 分子大小在变 |
| D | 液态水与水蒸气的化学性质相同 | 同种分子性质相同 |
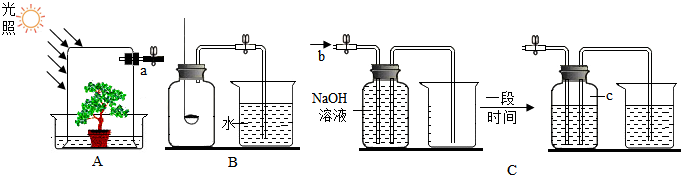
10.某课外小组的同学将玻璃罩内充满纯净的二氧化碳气体,如图A所示,在光照充足的条件下,经过一段时间后,该小组同学用注射器从a处抽取气体,测定玻璃罩内气体的成分及其含量.
【查阅资料】
①植物通过光合作用吸收二氧化碳气体,放出氧气.
②氢氧化钠和氢氧化钙性质相似,其水溶液都能与二氧化碳发生反应,且没有气体物质生成.
【实验一】检验玻璃罩内是否含有二氧化碳气体?
【实验二】采用两种方法测定玻璃罩内气体中氧气的含量.
方法1:用如图B所示的装置测量气体中氧气的含量.
(1)将抽取出的气体用排水法收集到150mL的集气瓶中,燃烧匙中点燃的固体药品的名称是红磷;其燃烧现象为产生大量的白烟;反应方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)待装置冷却到室温后,打开弹簧夹,烧杯中的液体进入集气瓶中,其原因是氧气在磷燃烧中被消耗,在大气压强的作用下烧杯中的液体进入集气瓶中;
(3)实验结束后,集气瓶中进入液体的体积约为125mL.
方法2:用如图C所示的装置测量气体中氧气的含量.
(1)抽取150mL的气体,缓缓地从b处通入装置中;
(2)实验结束后,c处气体的化学式为O2,集气瓶中排出液体的体积约为75mL.
【实验二讨论】通过对比,该小组同学发现,两种方法所得实验结果差距较大,其中实验结果更准确的是方法2(填写“方法1”或“方法2”),该方法所测得氧气约占气体总体积的50%.另一实验方法中不合理的实验操作是方法1,装置冷却后,进入的水中含有二氧化碳(友情提示:请注明是哪种方法).

【查阅资料】
①植物通过光合作用吸收二氧化碳气体,放出氧气.
②氢氧化钠和氢氧化钙性质相似,其水溶液都能与二氧化碳发生反应,且没有气体物质生成.
【实验一】检验玻璃罩内是否含有二氧化碳气体?
| 实验步骤 | 实验现象 | 实验结论 |
| 抽取适量气体,注入澄清石灰水中 | 有白色沉淀产生 | 玻璃罩内含有二氧化碳气体 |
方法1:用如图B所示的装置测量气体中氧气的含量.
(1)将抽取出的气体用排水法收集到150mL的集气瓶中,燃烧匙中点燃的固体药品的名称是红磷;其燃烧现象为产生大量的白烟;反应方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)待装置冷却到室温后,打开弹簧夹,烧杯中的液体进入集气瓶中,其原因是氧气在磷燃烧中被消耗,在大气压强的作用下烧杯中的液体进入集气瓶中;
(3)实验结束后,集气瓶中进入液体的体积约为125mL.
方法2:用如图C所示的装置测量气体中氧气的含量.
(1)抽取150mL的气体,缓缓地从b处通入装置中;
(2)实验结束后,c处气体的化学式为O2,集气瓶中排出液体的体积约为75mL.
【实验二讨论】通过对比,该小组同学发现,两种方法所得实验结果差距较大,其中实验结果更准确的是方法2(填写“方法1”或“方法2”),该方法所测得氧气约占气体总体积的50%.另一实验方法中不合理的实验操作是方法1,装置冷却后,进入的水中含有二氧化碳(友情提示:请注明是哪种方法).
11.我们接触过的有些化学反应是无明显现象的.如图三个实验都是通过滴加其他试剂的方法,使之产生明显的现象,以证明反应确实发生了.请回答下列问题.

(1)实验甲中能证明反应发生的现象是溶液由红色变为无色,该现象可说明反应后的溶液中一定
不含有的溶质是氢氧化钠.
(2)从研究原理得知,实验乙可通过滴加酸碱指示剂的方法证明反应发生了,实验乙中选用的酸碱指示剂是紫色石蕊试液.请写出实验乙中反应的化学方程式CO2+H2O=H2CO3.
(3)实验丙中,玲玲同学选用了两种不同类别的试剂都证明了氢氧化钠溶液和二氧化碳能发生反应.请
你帮她把实验报告补充完整.
实验结束后,同学们对反应后所得溶液的成分展开了讨论.方案一最终所得溶液中的溶质是氯化钠和氯化氢.

(1)实验甲中能证明反应发生的现象是溶液由红色变为无色,该现象可说明反应后的溶液中一定
不含有的溶质是氢氧化钠.
(2)从研究原理得知,实验乙可通过滴加酸碱指示剂的方法证明反应发生了,实验乙中选用的酸碱指示剂是紫色石蕊试液.请写出实验乙中反应的化学方程式CO2+H2O=H2CO3.
(3)实验丙中,玲玲同学选用了两种不同类别的试剂都证明了氢氧化钠溶液和二氧化碳能发生反应.请
你帮她把实验报告补充完整.
| 方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取通入二氧化碳后的溶液少量于试管中,滴加过量的稀盐酸 | 有气泡产生 | 氢氧化钠溶液和二 氧化碳能发生反应 |
| 方案二 | 取通入二氧化碳后的溶液少量于试管中,滴加少量的氢氧化钙溶液 | 产生白色沉淀 |