题目内容
11.碳酸亚铁(FeCO3)是生产补血剂的原料.以下是某同学设计的利用铁矿烧渣(主要成分是 Fe2O3、FeO和泥沙等)制取碳酸亚铁的实验流程图: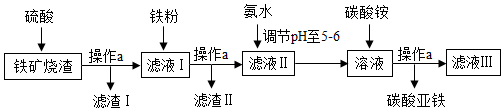
请回答下列问题:
(1)操作a中需要用到的玻璃仪器主要有烧杯、玻璃棒和漏斗;
(2)滤液Ⅰ中含有的金属阳离子:Fe2+、Fe3+(填离子符号);
(3)滤液Ⅰ中加入铁粉后可能发生的化学反应方程式:①Fe+H2SO4=FeSO4+H2↑;②Fe2(SO4)3+Fe=3FeSO4;
(4)加入碳酸铵得到碳酸亚铁的反应化学方程式:(NH4)2CO3+FeSO4=FeCO3↓+(NH4)2SO4.
分析 (1)根据题目给出的流程图和信息可知,操作a是将固液分开,操作是过滤,据此分用到的仪器;
(2)根据硫酸与Fe2O3、FeO的反应分析滤液Ⅰ中含有的金属阳离子;
(3)滤液Ⅰ中加入铁粉后能与剩余的硫酸反应,能与硫酸铁反应,据此写出反应的化学方程式;
(4)根据碳酸铵和和硫酸亚铁反应写出反应的化学方程式.
解答 解:(1)由流程图可知,操作a是将固液分开,操作是过滤,需要用到的玻璃仪器主要有烧杯、玻璃棒和漏斗;
(2)由于硫酸能与氧化亚铁反应生成了硫酸亚铁和水,能与氧化铁反应生成了硫酸铁和水,所以滤液Ⅰ中含有的金属阳离子:Fe2+、Fe3+;
(3)滤液Ⅰ中加入铁粉后可能发生的是铁能与硫酸反应生成了硫酸亚铁和氢气、能与硫酸铁反应和生成硫酸亚铁,反应的化学方程式分别是:Fe+H2SO4=FeSO4+H2↑,Fe2(SO4)3+Fe=3FeSO4;
(4)碳酸铵和硫酸亚铁反应生成碳酸亚铁白色沉淀和硫酸铵,反应的化学方程式是:(NH4)2CO3+FeSO4=FeCO3↓+(NH4)2SO4.
故答为:(1)漏斗;(2)Fe3+;(3)Fe2(SO4)3+Fe=3FeSO4;(4)(NH4)2CO3+FeSO4=FeCO3↓+(NH4)2SO4.
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
19.下列实验操作中净水程度最高的是( )
| A. | 静置 | B. | 过滤 | C. | 煮沸 | D. | 蒸馏 |
3.用石灰石和稀盐酸制二氧化碳后所得的溶液中一定含有的溶质是( )
| A. | CaCl2 | B. | HCl | C. | CaCl2和CaCO3 | D. | HCl和CaCl2 |
20. 如图中甲、乙、丙、X分别是Fe2O3、C、CO、盐酸中的某一种,甲、乙、丙均能与X发生化学反应,则X是( )
如图中甲、乙、丙、X分别是Fe2O3、C、CO、盐酸中的某一种,甲、乙、丙均能与X发生化学反应,则X是( )
 如图中甲、乙、丙、X分别是Fe2O3、C、CO、盐酸中的某一种,甲、乙、丙均能与X发生化学反应,则X是( )
如图中甲、乙、丙、X分别是Fe2O3、C、CO、盐酸中的某一种,甲、乙、丙均能与X发生化学反应,则X是( )| A. | Fe2O3 | B. | CO | C. | 盐酸 | D. | C |
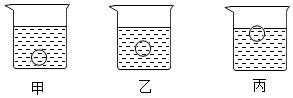 如图,把一木块漂浮在80℃的饱和硫酸铜溶液中,当溶液温度逐渐降低到20℃的过程中,会看到烧杯底部有蓝色晶体析出,说明硫酸铜的溶解度会随着温度的升高而增大,同时仔细观察会发现木块下沉(填“上浮”或“下沉”)一些.
如图,把一木块漂浮在80℃的饱和硫酸铜溶液中,当溶液温度逐渐降低到20℃的过程中,会看到烧杯底部有蓝色晶体析出,说明硫酸铜的溶解度会随着温度的升高而增大,同时仔细观察会发现木块下沉(填“上浮”或“下沉”)一些.