题目内容
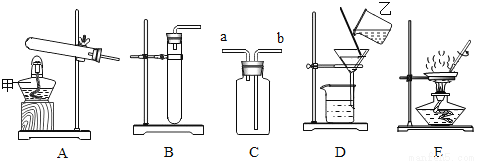
在盛有少量稀盐酸的烧杯中加入足量的碳酸镁固体至恰好完全反应。请回答:
(1)上述反应中的实验现象为___________________________。
(2)下图表示加入碳酸镁固体前后溶液中存在的主要离子,写出每种图形代表的离子
(写离子符号)。
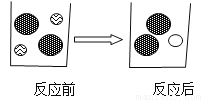
 __________,
__________, __________,
__________,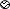 ____________。
____________。
(3)下列物质中能与盐酸反应,而且反应前后溶液中的离子种类和个数比变化与上图相似的是_________________(填序号)。
A.CuO粉末 B.KOH溶液 C. BaCO3固体 D.Cu片
固体逐渐溶解,有气泡产生 Cl- Mg2+ H + AC 【解析】(1)碳酸镁和盐酸反应生成氯化镁、水和二氧化碳,所以反应中的实验现象为固体逐渐溶解,有气泡产生; (2)碳酸镁和盐酸反应生成氯化镁、水和二氧化碳,加入碳酸镁固体前,溶液中含有大量的氢离子、氯离子,加入后,溶液中含有大量的镁离子、氯离子;所以表示氯离子,表示镁离子,表示氢离子; (3)A、氧化铜与盐酸反应生成氯化铜和...
练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
经过一年的化学学习,小宇同学对以下所学知识进行整理,正确的是:
A | 不同物质性质不同,鉴别方法不同 | 氧化铜与碳粉一一在空气中灼烧 |
B | 物质在微观上都是由粒子构成的 | 铁一一由分子构成 |
C | 物质的性质决定了它的反应现象 | 向Na0H溶液中滴加紫色石蕊试液一一溶液变为红色 |
D | 混合物除去杂质(括号内为杂质) | FeS04溶液(稀H2S04)一一加入过量的氧化铁,过滤 |
A. A B. B C. C D. D
A 【解析】A、不同物质性质不同,鉴别方法不同,碳粉在空气中灼烧会生成二氧化碳,并有火星出现,氧化铜不反应,故正确; B、金属铁由原子直接构成,故错误; C、NaOH溶液显碱性,可以使紫色石蕊试液变为蓝色,故错误; D、氧化铁与硫酸反应生成硫酸铁,又形成新的杂质,不符合除杂原理,故错误。除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是
选项 | 物质 | 选用试剂 | 操作方法 |
A | Fe2O3(Fe) | 盐酸 | 浸泡、过滤、洗涤、烘干 |
B | CO(CO2) | NaOH溶液、浓硫酸 | 洗气、干燥 |
C | CaO(CaCO3) | 水 | 过滤、烘干 |
D | NaCl(Na2CO3) | Ca(NO3)2溶液 | 溶解、过滤、蒸发、结晶 |
A. A B. B C. C D. D
B 【解析】除去杂质的原则是所加试剂只与杂质反应,且不生成新的杂质。A、盐酸也能与氧化铁反应,错误;B、混合气体通过氢氧化钠溶液,可除去二氧化碳气体,再通过浓硫酸除去气体中的水蒸气,正确;C、氧化钙能与水反应,错误;D、Ca(NO3)2+Na2CO3=CaCO3↓+2NaNO3引入杂质硝酸钠,错误。故选B。