题目内容
17.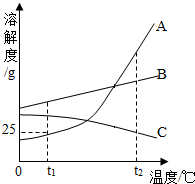 如图是A、B、C三种固体物质在水中的溶解度曲线图,请回答下列问题:
如图是A、B、C三种固体物质在水中的溶解度曲线图,请回答下列问题:(1)t1℃时A物质的溶解度是25克.
(2)当A物质中混有少量B物质吋,通常可采用降温结晶的方法提纯A物质.
(3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃后(升温过程中溶剂的质量不变),三种溶液中溶质的质量分数由大到小的顺序是B>C>A(填字母).
分析 根据已有的溶解度曲线的意义进行分析解答,交点表示在同一温度下两种物质的溶解度相等,可以比较同一温度下两种物质的溶解度的大小,根据溶解度随温度的变化特点确定析出晶体的方法,根据溶质质量分数进行比较即可.
解答 解:(1)据图可以看出,t1℃时A物质的溶解度是25g,故填:25;
(2)A物质的溶解度随温度的升高变化大,当A物质中混有少量B物质吋,通常可采用降温结晶的方法提纯A物质,故填:降温结晶;
(3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃后,AB的溶解度随温度的升高而增大,故溶液组成不变,溶质质量分数与t1℃相同,且是B大于A,C的溶解度随温度的升高而减小,会析出固体,据图可以看出,C的溶质质量分数大于A,故三种溶液中溶质的质量分数由大到小的顺序是B>C>A,故填:B>C>A.
点评 本考点考查了溶解度曲线及其应用,完成此题,可以依据已有的溶解度曲线的意义进行,通过溶解度曲线我们可以获得很多信息;本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
7.下列有关溶液的说法正确的是( )
| A. | 形成溶液的溶质都是固态物质 | |
| B. | 饱和溶液的质量分数一定比不饱和溶液的质量分数大 | |
| C. | 溶液具有均一性和稳定性 | |
| D. | 所有物质溶于水形成溶液都要吸收热量 |
8.向CuO和铁粉的混合物中加入一定量的稀硫酸,微热,充分反应后冷却、过滤,在滤液中放入一枚洁净的铁钉.发现铁钉表面无任何变化,据此判断,下列结论正确的是( )
| A. | 滤液中一定含有FeSO4,可能含有H2SO4 | |
| B. | 滤液中可能有CuSO4 | |
| C. | 滤渣里一定有Cu,可能有Fe和CuO | |
| D. | 滤渣里一定有Cu和Fe |
5.下列的符号中,既能表示一种元素,又能表示该元素的一个原子,还表示一种元素的单质的是( )
| A. | Ar | B. | N | C. | F | D. | CO |
12.氢氧化铝作为阻燃剂受热分解时吸收热量,同时生成耐高温的氧化铝和大量水蒸气,起到防火作用.下列叙述错误的是( )
| A. | 反应吸热,降低了可燃物的着火点 | |
| B. | 生成氧化铝覆盖在可燃物表面,隔绝空气 | |
| C. | 生成大量水蒸气,降低可燃物周围氧气的浓度 | |
| D. | 反应能够降低温度,可燃物不易达到着火点 |
9.生活中的下列变化不属于化学变化的是( )
| A. | 铁器生锈 | B. | 葡萄酿酒 | C. | 剩饭变馊 | D. | 苹果榨汁 |
6.下列物质放入水中,不能形成溶液的是( )
| A. | 蔗糖 | B. | 植物油 | C. | 食盐 | D. | 食用纯碱 |
8.为除去物质中的杂质,所选试剂(过量)及操作方法均正确的是( )
| 选项 | 物质 | 杂质 | 除去杂质的试剂或方法 |
| A | 氧化钙 | 碳酸钙 | 加水溶解后过滤 |
| B | 二氧化碳 | 氯化氢 | 通过氢氧化钠溶液的洗气瓶 |
| C | 硝酸铜溶液 | 硝酸银溶液 | 加入铜粉过滤 |
| D | 硫酸钠溶液 | 稀硫酸 | 加入碳酸钠溶液 |
| A. | A | B. | B | C. | C | D. | D |