题目内容
17.下列除去杂质的方法中错误的是| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | O2 | CO | 通过灼热的氧化铜 |
| B | KNO3体 | NaCl固体 | 热水溶解、降温结晶、过滤 |
| C | NaCl固体 | Na2CO3 固体 | 过量稀盐酸、蒸发结晶 |
| D | CaCl2溶液 | 稀盐酸 | 过量碳酸钙、过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO能与灼热的氧化铜反应生成铜和二氧化碳,但一氧化碳与氧气的混合气体在加热时易发生爆炸,不符合除杂原则,故选项所采取的方法错误.
B、KNO3和NaCl的溶解度受温度的影响不同,硝酸钾溶解度受温度影响较大,而氯化钠受温度影响较小,所以可采取加热水溶解配成饱和溶液、冷却热饱和溶液使KNO3先结晶出来、再过滤的方法;故选项所采取的方法正确.
C、Na2CO3固体能与过量稀盐酸反应生成氯化钠、水和二氧化碳,再蒸发结晶,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、稀盐酸能与过量的碳酸钙反应生成氯化钙、水和二氧化碳,再过滤除去过量的碳酸钙,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:A.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
7.煤、石油、天然气是重要的化石燃料.下列关于化石燃料的叙述错误的是( )
| A. | 石油是一种重要的化工原料 | B. | 石油分馏可得到多种产品 | ||
| C. | 煤、石油、天然气是可再生能源 | D. | 煤被称为“工业的粮食” |
8.杯中的某种溶液,倒掉一半后,剩下的半杯溶液的描述正确的是( )
| A. | 比热容减半 | B. | 密度减半 | ||
| C. | 质量减半 | D. | 溶质质量分数减半 |
5.氢元素有3种不同的原子,其原子核内的中子数依次为 0、1、2.这3种原子与金属 锂形成的氢化锂“三兄弟”LiH、LiD、LiT 是“神舟七号”的燃料.下列说法正确的是( )
| A. | H、D、T 相对原子质量之比为 1:2:3 | |
| B. | LiH、LiD、LiT 相对分子质量相同 | |
| C. | H、D、T 化学性质不同 | |
| D. | LiH、LiD、LiT 中 Li 元素质量分数相等 |
12.人们的衣食住行都离不开材料.下列生活用品所含的主要材料,属于合成材料的是( )
| A. | 铁锅 | B. | 瓷碗 | C. | 塑料盆 | D. | 玻璃杯 |
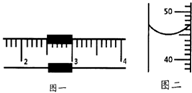 实验室需配制一定溶质质量分数的氯化钠溶液.
实验室需配制一定溶质质量分数的氯化钠溶液.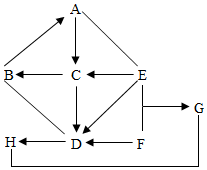 已知A~H八种物质均为初中化学常见物质,A、B、E、F为不同类别的化合物,B、D、G为氧化物,B为常用食品干燥剂,D在常温下为液态,E为常用洗涤剂,G、H为无色气体.F为胃酸的主要成分.A、B、E放入水中能使酚酞变红,如图是它们之间的关系 (部分反应物和产物已省略;“→”表示转化,“-”表示相互反应),请回答:
已知A~H八种物质均为初中化学常见物质,A、B、E、F为不同类别的化合物,B、D、G为氧化物,B为常用食品干燥剂,D在常温下为液态,E为常用洗涤剂,G、H为无色气体.F为胃酸的主要成分.A、B、E放入水中能使酚酞变红,如图是它们之间的关系 (部分反应物和产物已省略;“→”表示转化,“-”表示相互反应),请回答: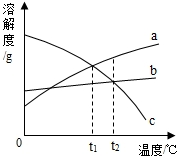 如图是a,b,c三种固体物质的溶解度曲线.据图回答:
如图是a,b,c三种固体物质的溶解度曲线.据图回答: