题目内容
今有氢气和氧气的混合气体10g,点燃充分燃烧,恢复到室温,气体质量减少了9g,则原混合气体中氢气的质量可能为( )
| A、1g | B、3g | C、4g | D、5g |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:由题意“氢气和氧气的混合气体10g,点燃充分燃烧后,恢复到室温,气体质量减少了9g”,说明反应的气体质量为9克,剩余气体1g,则根据质量守恒定律可知生成水的质量9g,利用化学反应方程式可知,可求出参加反应氢气和氧气的质量来分析解答.
解答:解:充分燃烧,恢复到室温,气体质量减少了9g,由质量守恒定律可知生成水的质量9g.
设参加反应反应的氢气和氧气的质量分别为x、y;
2H2+O2
2H2O
4 32 36
x y 9g
=
=
x=1g y=8g
剩余气体1g,若为氢气,则原混合气体中氢气的质量可能为1g+1g=2g;若为氧气,则原混合气体中氢气的质量可能为1g;
答案:A
设参加反应反应的氢气和氧气的质量分别为x、y;
2H2+O2
| ||
4 32 36
x y 9g
| 4 |
| x |
| 32 |
| y |
| 36 |
| 9g |
x=1g y=8g
剩余气体1g,若为氢气,则原混合气体中氢气的质量可能为1g+1g=2g;若为氧气,则原混合气体中氢气的质量可能为1g;
答案:A
点评:掌握质量守恒定律的内容及其应用;掌握根据化学反应的化学方程式计算的方法.在解此类题时,首先根据题中的条件列出关系式,解出题中需要的量,然后结合题意在进一步解答.

练习册系列答案
相关题目
名称中有“水”字的物质可能是溶液,下列有“水”字的物质不属于溶液的是( )
| A、糖水 | B、食盐水 |
| C、蒸馏水 | D、澄清的石灰水 |
近期,人类解决水危机的方法是( )
| A、节约用水,合理用水 |
| B、用海水灌溉农田 |
| C、大量开采地下水 |
| D、海水淡化 |
下列微粒符号中,对“2”含义的理解正确的是( )
| A、2Cu中的“2”表示2个铜元素 |
| B、Fe2+中的“2”表示每个铁离子带有2个单位的正电荷 |
| C、H2O中的“2”表示一个水分子中含有两个氢原子 |
| D、O2 中的“2”表示2个氧原子 |
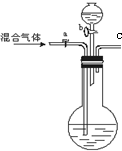 有CO2和CO组成的混合气体,为了将他们分开,有同学设计了如图的实验装置.图中烧瓶中盛的是足量澄清石灰水,分液漏斗中盛的是稀盐酸.
有CO2和CO组成的混合气体,为了将他们分开,有同学设计了如图的实验装置.图中烧瓶中盛的是足量澄清石灰水,分液漏斗中盛的是稀盐酸.