题目内容
11.过氧乙酸是较为有效的一种消毒剂,其化学式为C2H4O3,请回答:(1)该物质由三 种元素组成的,各元素的原子个数比C:H:O为2:4:3,过氧乙酸的相对分子质量为76.
(2)过氧乙酸中碳元素的质量分数是多少?31.6%(结果精确到0.1% )
(3)38g过氧乙酸中含碳元素的质量是多少克?12g.
分析 (1)根据化学式的意义以及相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中元素质量分数的计算方法来分析;
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)由过氧乙酸的化学式可知,过氧乙酸是由碳、氢、氧三种元素组成的;一个过氧乙酸分子是由2个碳原子、4个氢原子和3个氧原子构成的,则该物质的一个分子有9个原子,各元素的原子个数比C:H:O为2:4:3;过氧乙酸的相对分子质量为12×2+1×4+16×3=76.故填:三;2:4:3;76;
(2)过氧乙酸中碳元素的质量分数是$\frac{12×2}{76}×100%$≈31.6%.故填:31.6%;
(3)38g过氧乙酸中含碳元素的质量是38g×$\frac{12×2}{76}×100%$=12g;故填:12.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
2.6月5日是世界环境日,今年中国的主题是“绿水青山就是金山银山”.下列说法不符合这一主题的是( )
| A. | 植树造林 | B. | 双面使用纸张 | ||
| C. | 回收废弃塑料 | D. | 生活污水任意排放 |
19.将燃着的镁带伸入盛满二氧化碳的集气瓶中,镁带继续剧烈燃烧,生成氧化镁和碳.下列叙述错误的是( )
| A. | 该反应中元素的化合价发生了改变 | |
| B. | 燃烧并不一定需要氧气 | |
| C. | 不能用二氧化碳来熄灭镁带燃烧的火焰 | |
| D. | 该反应中二氧化碳是还原剂 |
3.下列实验操作或实验正确的是( )
| A. | 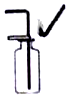 收集CO2并验满 | B. |  加入大理石 | C. | 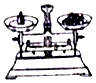 称量固体 | D. | 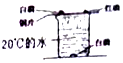 探究燃烧条件 |
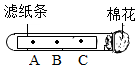 如图所示,在试管中的滤纸条上A、B、C三处各滴上一滴无色酚酞,再在试管口放一团棉花.
如图所示,在试管中的滤纸条上A、B、C三处各滴上一滴无色酚酞,再在试管口放一团棉花.



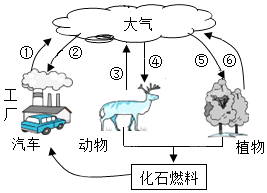 如图是自然界中碳、氧循环的示意图,其中箭头表示物质的转化方向.
如图是自然界中碳、氧循环的示意图,其中箭头表示物质的转化方向.