题目内容
(5分)小明了解到水龙头是铜质镀铬,好奇的小明想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀你一同参加:
【作出猜想】猜想1:Cr﹥Fe﹥Cu; 猜想2:Fe﹥Cu﹥Cr;猜想3:你的猜想
【查阅资料】(1)铬是有银白色金属光泽的金属,在空气中表面能生成致密的氧化膜。
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【设计与实验】小明取大小相等的三种金属片,用砂纸打磨光亮,再取三支试管,分别放入等量的同种稀硫酸。
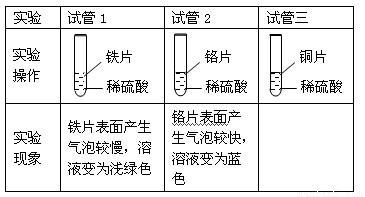
【结论解释】
(1)小明得到的结论是猜想 正确。
(2)将铬片投入FeSO4溶液中,反应 (填“能”或“不能”)进行。若能进行,请你写出反应的化学方程式: 。
【作出猜想】:Fe﹥Cr﹥Cu;【设计与实验】无明显现象;【结论解释】(1)1;(2)能 ;Cr + FeSO4===CrSO4+Fe
【解析】
试题分析:【作出猜想】:猜想3:Fe﹥Cr﹥Cu;【设计与实验】铜不稀硫酸不发生反应,无明显现象;【结论解释】(1)通过观察表格里内容,可知猜想1是正确的;(2)因为铬的活动性比铁强,所以能发生化学反应。
考点:金属活动性顺序的应用,化学方程式书写。

练习册系列答案
相关题目
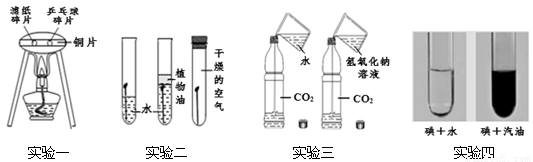
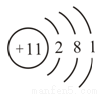
 2CO2+4H2O+3X,则X的化学式是 。
2CO2+4H2O+3X,则X的化学式是 。 H2↑+O2 ↑
H2↑+O2 ↑ 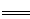 Fe2(SO4)3+3H2↑
Fe2(SO4)3+3H2↑