题目内容
8.现有A、B、C、D四瓶无色溶液,已知它们是盐酸、稀硫酸、碳酸钠和澄清石灰水,为了确定它们各是哪一种,做如下两个实验.①取A、B、C、D溶液样品各少许,两两混合,可观察到下列现象:
B跟D:产生白色沉淀;
A跟D、D跟C都产生气体.
②取A、C溶液样品少许,分别加入氯化钡溶液,A中无明显现象;C中产生白色沉淀.
根据上述实验现象推断,写出A、B、C、D四种物质的化学式.
A:HCl;B:Ca(OH)2;C:H2SO4;D:Na2CO3.
分析 根据题意,B跟D混合产生白色沉淀,A跟D、D跟C都产生气体,结合稀盐酸、稀硫酸能与碳酸钠溶液反应生成二氧化碳气体,则D为碳酸钠溶液;碳酸钠能与石灰水反应生成碳酸钙白色沉淀,则B为石灰水;取A、C溶液样品少许,分别加入氯化钡溶液,A中无明显现象,C中产生白色沉淀,结合硫酸能与氯化钡溶液反应生成硫酸钡白色沉淀,与稀盐酸不反应,则A为稀盐酸,C为硫酸;据此进行分析解答.
解答 解:由题意,A、B、C、D四瓶无色溶液,已知它们是盐酸、稀硫酸、碳酸钠和澄清石灰水;B跟D混合产生白色沉淀,A跟D、D跟C都产生气体,结合稀盐酸、稀硫酸能与碳酸钠溶液反应生成二氧化碳气体,则D为碳酸钠溶液;碳酸钠能与石灰水反应生成碳酸钙白色沉淀,则B为石灰水;取A、C溶液样品少许,分别加入氯化钡溶液,A中无明显现象,C中产生白色沉淀,结合硫酸能与氯化钡溶液反应生成硫酸钡白色沉淀,与稀盐酸不反应,则A为稀盐酸,C为硫酸.
A、B、C、D四种物质的化学式分别是HCl、Ca(OH)2、H2SO4、Na2CO3.
故答案为:HCl;Ca(OH)2;H2SO4;Na2CO3.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案
相关题目
11.实验是学习化学的重要途径,小亮在学习酸碱盐的化学性质时做了如下实验,请你和他一起完成实验活动.
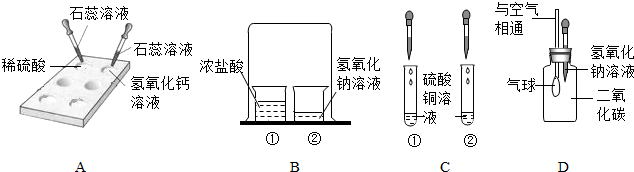
(1)在白色点滴板上完成实验A,请将实验现象补充完整.
(2)在实验B的烧杯②中滴加2滴酚酞溶液后,扣上大烧杯,一段时间后看到的现象是氢氧化钠溶液由红色变成无色,得出的结论是浓盐酸具有挥发性,酸碱会发生中和反应.
(3)在实验C的试管①中,滴加少量的氢氧化钠溶液,看到的现象是有蓝色沉淀生成,反应的化学方程式是2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.要使试管②中产生白色沉淀,应滴加氯化钡溶液(写一种溶液).
(4)小亮用实验D验证二氧化碳与氢氧化钠溶液反应,看到的现象是气球胀大,他根据三氧化硫与二氧化碳所属的类别,推断三氧化硫也能与氢氧化钠溶液反应,反应的化学方程式为SO3+2NaOH=Na2SO4+H2O.

(1)在白色点滴板上完成实验A,请将实验现象补充完整.
| 稀硫酸 | 氢氧化钙溶液 | |
| 实验现象 | 溶液变红色 | 溶液变蓝色 |
(3)在实验C的试管①中,滴加少量的氢氧化钠溶液,看到的现象是有蓝色沉淀生成,反应的化学方程式是2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.要使试管②中产生白色沉淀,应滴加氯化钡溶液(写一种溶液).
(4)小亮用实验D验证二氧化碳与氢氧化钠溶液反应,看到的现象是气球胀大,他根据三氧化硫与二氧化碳所属的类别,推断三氧化硫也能与氢氧化钠溶液反应,反应的化学方程式为SO3+2NaOH=Na2SO4+H2O.
3.常温下,下列说法错误的是( )
| A. | 溶液的pH由5变成2,其酸性减弱 | |
| B. | pH=7的溶液显中性 | |
| C. | pH=2的溶液显酸性 | |
| D. | pH>10的土壤不适于种植农作物,因为碱性太强 |
20.下列说法正确的是( )
| A. | 可用熟石灰改良酸性土壤 | |
| B. | 晚上天然气泄露,应立即开灯查找原因 | |
| C. | 不能用燃烧的方法区分羊毛和涤纶 | |
| D. | 食用加碘盐可补充常量元素碘 |
17.将化学知道用到生产、生活中,是学习化学的目的之一.不列做法中正确的是( )
| A. | 大量用塑料袋包装食品 | B. | 用水经常冲洗自行车以防止生锈 | ||
| C. | 炒菜时油锅着火,立即盖上锅盖 | D. | 绝对不许施用化肥、农药 |
18.泸州又称酒城,盛产白酒.根据物质的分类方法,判断白酒属于( )
| A. | 单质 | B. | 化合物 | C. | 氧化物 | D. | 混合物 |