题目内容
8.实验室需要配制15%的氯化钠溶液50g.(1)计算:需氯化钠的质量为7.5g
(2)某同学按下图所示步骤依次操作:

其中操作错误的步骤是A、B填字母序号);B中仪器的名称为量筒;E中玻璃棒的作用是加速溶解.
(3)若上图A中砝码的质量为5g,游码的读数为2.5g,则小明称得的氯化钠质量实际为2.5g.
分析 (1)根据溶质质量分数公式可以计算出所需氯化钠的质量解答;
(2)根据用托盘天平时应左物右码,量筒读数时应使视线与凹液面的最低处保持水平解答;
(3)根据根据天平的使用方法是左物右码,左盘的质量等于右盘的质量加游码的质量,即药品质量=砝码质量+游码质量,如果位置放反,根据左盘的质量=右盘的质量+游码的质量,列等式进行计算.
解答 解:
(1)需氯化钠的质量为50 g×15%=7.5 g;
(2)使用托盘天平时应左物右码,量筒读数时应使视线与凹液面的最低处保持水平,在此实验中玻璃棒的作用为搅拌,其目的为加速溶解;
(3)托盘天平中左盘的质量=右盘的质量+游码的质量,因为称量时药品与砝码放反了,所以药品的实际质量为5 g-2.5 g=2.5 g.
答案:
(1)7.5 g;
(2)A、B;量筒;加速溶解;
(3)2.5 g
点评 本题考查的是溶液的配制,完成此题,可以依据已有的知识进行回答,所以要求同学们在平时的学习中要加强基础知识的储备.

练习册系列答案
相关题目
18.下列仪器不是用于存放药品的是( )
| A. | 广口瓶 | B. | 细口瓶 | C. | 滴瓶 | D. | 锥形瓶 |
19.小明的作业有以下表述,其中错误的是( )
| A. | 氧气是由氧分子构成的 | |
| B. | 汞是由汞原子构成的 | |
| C. | 氯化钠是由钠离子和氯离子构成的 | |
| D. | 二氧化碳是由一个碳元素和两个氧元素构成的 |
16.在2X+Y2═2Z的反应中,X的相对原子质量为24,Y2的相对分子质量为32,Z的相对分子质量为( )
| A. | 32 | B. | 40 | C. | 56 | D. | 64 |
3. “科学是一把双刃剑”,化学尤其如此.它既可以给人类带来巨大的物质财富,提高人类的生活质量,也可以给人类带来灾难.“白色污染”这个概念是20世纪90年代初由我国提出来的,但是这一警示很快得到国际社会的认同.“白色污染”是( )
“科学是一把双刃剑”,化学尤其如此.它既可以给人类带来巨大的物质财富,提高人类的生活质量,也可以给人类带来灾难.“白色污染”这个概念是20世纪90年代初由我国提出来的,但是这一警示很快得到国际社会的认同.“白色污染”是( )
 “科学是一把双刃剑”,化学尤其如此.它既可以给人类带来巨大的物质财富,提高人类的生活质量,也可以给人类带来灾难.“白色污染”这个概念是20世纪90年代初由我国提出来的,但是这一警示很快得到国际社会的认同.“白色污染”是( )
“科学是一把双刃剑”,化学尤其如此.它既可以给人类带来巨大的物质财富,提高人类的生活质量,也可以给人类带来灾难.“白色污染”这个概念是20世纪90年代初由我国提出来的,但是这一警示很快得到国际社会的认同.“白色污染”是( )| A. | 冶炼厂的白色烟尘 | B. | 石灰窑的白色粉末 | ||
| C. | 各类塑料垃圾 | D. | 白色建筑材料产生的建筑垃圾 |
18.下列做法能达到目的是( )
| A. | 向某无色未知溶液中加入BaCl2溶液产生白色沉淀,证明存在SO42- | |
| B. | 用氢氧化钠溶液证明一氧化碳气体中是否含有二氧化碳 | |
| C. | 清洗试管中附着的氢氧化铜:先向试管中注入稀硫酸,振荡,再用蒸馏水冲洗 | |
| D. | 鉴别硫酸铵和氯化铵两种氮肥:分别与熟石灰混合后研磨,闻气味 |
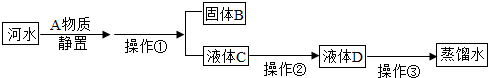
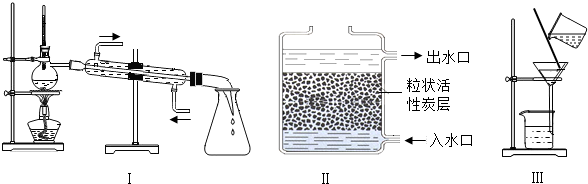
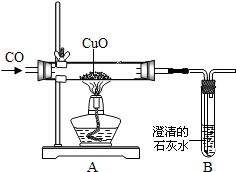 一氧化碳是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题:
一氧化碳是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题: