题目内容
18.3月15日,央视《每周质量报告》报道:一些企业用皮革废料熬制工业明胶,在加工过程中添加重铭酸钾.在加热条件下重铬酸钾分解,反应的化学方程式为:4K2Cr2O7$\frac{\underline{\;\;△\;\;}}{\;}$4K2CrO4+2X+3O2↑,工业明胶制造药用胶囊,导致胶囊重金属铬超标.铬是一种重金属元素,能对肝、肾等内脏器官和DNA造成损伤.在通常情况下,铬单质是银白色金属光泽的固体,有较高的熔点,是最硬的金属;在加热时,能与浓硫酸反应生成硫酸铬(其中铬元素化合价为+3价),同时还生成一种大气污染物和一种常见的液体.(1)K2Cr2O7中铬元素的化合价是+6;K2Cr2O7分解生成X的化学式为Cr2O3;
(2)铬单质与浓硫酸反应的化学方程式为2Cr+6H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Cr2(SO4)3+6H2O+3SO2↑.
分析 (1)根据在化合物中正负化合价代数和为零,结合K2Cr2O7的化学式进行解答即可.
由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
(2)在加热时,铬单质与浓硫酸反应生成硫酸铬(其中铬元素化合价为+3价),同时还生成一种大气污染物和一种常见的液体,由质量守恒定律,反应前后元素种类不变,则大气污染物和一种常见的液体,分别是二氧化硫、水,写出反应的化学方程式即可.
解答 解:(1)钾元素显+1价,氧元素显-2价,设铬元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+2x+(-2)×7=0,则x=+6价.
由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式4K2Cr2O7$\frac{\underline{\;\;△\;\;}}{\;}$4K2CrO4+2X+3O2↑,反应前钾、铬、氧原子个数分别为8、8、28,反应后的生成物中钾、铬、氧原子个数分别为8、4、22,根据反应前后原子种类、数目不变,则2X分子中含有4个铬原子和6个氧原子,则每个X分子由2个铬原子和3个氧原子构成,则物质X的化学式为Cr2O3.
(2)在加热时,铬单质与浓硫酸反应生成硫酸铬(其中铬元素化合价为+3价),同时还生成一种大气污染物和一种常见的液体,由质量守恒定律,反应前后元素种类不变,则大气污染物和一种常见的液体,分别是二氧化硫、水,反应的化学方程式为:2Cr+6H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Cr2(SO4)3+6H2O+3SO2↑.
故答案为:(1)+6;(2)Cr2O3;(3)2Cr+6H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Cr2(SO4)3+6H2O+3SO2↑.
点评 本题难度不大,掌握化合物中正负化合价代数和为零、化学反应前后原子守恒、化学方程式的书写方法是正确解答本题的关键.

 阅读快车系列答案
阅读快车系列答案| A. | 空气的成分按体积计算氮气最多 | |
| B. | 催化剂只能加快化学反应速率 | |
| C. | 植物叶片发黄应施加磷肥 | |
| D. | 碳酸氢钠俗称苏打,是发酵粉成分之一 |
| A. |  称量 | B. | 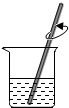 溶解 | C. | 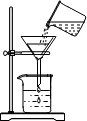 过滤 | D. | 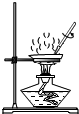 蒸发 |
| A. | 消除可燃物 | B. | 隔绝空气 | C. | 降低温度 | D. | 降低着火点 |
| A. | 篮球架的表面喷涂油漆,只是为了美观 | |
| B. | 不锈钢抗腐蚀性好,常用于制医疗器械,炊具等 | |
| C. | 回收金属饮料罐,只是为了减少环境污染 | |
| D. | 银的导电性比铜好,所以常用银作电线而不用铜 |
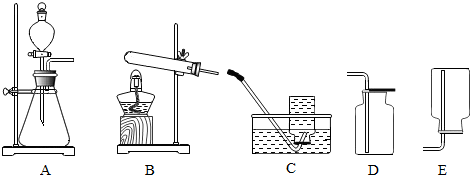
 如图为某制药厂生产的高钙片标签上的部分文字,请阅读后回答:
如图为某制药厂生产的高钙片标签上的部分文字,请阅读后回答: