题目内容
请结合下图回答问题:
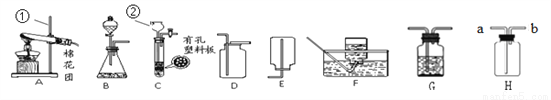
(1)写出图中有标号仪器的名称:①__________,② ___________。
(2)用加热高锰酸钾的方法制取氧气,应选用的发生装置是(填字母编号)_______,装入药品前应先_______,写出该反应化学方程式_____________________。
(3)用B、D装置组合制取二氧化碳气体的化学方程式___________________________。 若要获得干燥的该气体,除发生、收集装置外,还应选用G装置,并在该装置中盛放_______(填名称)。如果用H装置收集该气体,则气体从_______________端进入(填“a”或“b”)。
(4)实验室用锌粒和稀硫酸反应制取H2的化学方程式___________________,常选用装置B或C, C与B相比较,C的优点是_______________________________________
铁架台 长颈漏斗 A 检查装置的气密性 2KMnO4K2MnO4+MnO2+O2↑ CaCO3+2HCl=CaCl2+CO2↑+H2O 浓硫酸 a Zn + H2SO4=ZnSO4 + H2↑ 控制反应的发生与停止 【解析】(1)根据常见仪器解答;(2)根据反应物的状态、反应条件解答;根据装入药品前应先检查装置的气密性解答;根据高锰酸钾在加热的条件下分解生成锰酸钾、二氧化锰和氧气解答;(3)...
练习册系列答案
相关题目
某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。NaOH和Ca(OH)2的市场价格如表:
名称 | Ca(OH)2 | NaOH |
价格(元/kg) | 6.00 | 24.00 |
(1)若要清洗50kg这种石油产品,需要__________gNaOH?(写出计算步骤)
(2)石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。每处理50kg这种产品,可以节约______________元经费?
2kg 36.9 【解析】【解析】 (1)50千克石油产品所含的硫酸的质量为50kg×4.9%=2.45kg; (2)设需要的氢氧化钠的质量为x,需要的氢氧化钙的质量为y, 2NaOH+H2SO4=Na2SO4+2H2O 80 98 x 2.45kg x=2kg, Ca(OH)2+H2SO4=CaSO4+2H2O 74 98 y 2.45kg...

 ”中H正上方的“+1”表示 ,H右下角的“2”表示 。
”中H正上方的“+1”表示 ,H右下角的“2”表示 。
