题目内容
2.已知某CO和CO2的混合物中碳元素与氧元素的质量比为1:2.现将18g这种混合气体通过灼热的氧化铁(假设发生的反应物都充分进行),并将所得气体全部通入过量的澄清石灰水中,则石灰水减少的质量为( )| A. | 10g | B. | 28g | C. | 37g | D. | 50g |
分析 根据混合气体中碳元素的质量分数,计算出碳元素的质量,而这些质量的碳元素最终都会转化为二氧化碳,根据二氧化碳的质量可计算生成的碳酸钙的质量.
解答 解:碳元素的质量为:18g×$\frac{1}{3}$=6g,
C-CO2-CaCO3
12 100
6g 50g
通过关系式可以看出生成的二氧化碳质量为50g.
故选:D.
点评 本题不用分别计算出一氧化碳和二氧化碳的质量,只需知道不管是原来的二氧化碳,还是一氧化碳还原氧化铁生成的二氧化碳,其中含有的碳元素都来自原混合物中的碳.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如表:
根据质量守恒定律判断,X的值为( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/g | 20 | 55 | 20 | 70 |
| 反应后的质量/g | 0 | 95 | X | 5 |
| A. | 45 | B. | 65 | C. | 20 | D. | 40 |
14.国内外各大媒体曝光:某地山区生姜种植户,在种植生姜时使用了一种叫“神农丹”的剧毒农药.“神农丹”所含物质的化学式为C7H14N2O2S,下列关于该物质的说法,不正确的是( )
| A. | 该物质属于有机化合物 | |
| B. | 该物质的一个分子中含有26个原子 | |
| C. | 该物质中C、H、N、O、S五种元素的质量之比为7:14:2:2:1 | |
| D. | 该物质氢元素的含量最低 |
11.t2℃时,将甲、乙固体各W g (不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,降温到t1℃时现象如图2(水分不蒸发),甲、乙固体的溶解度曲线如图3.
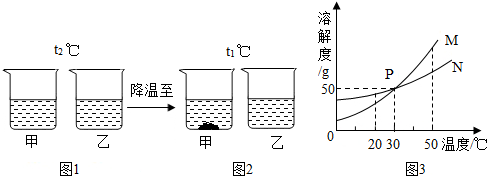
下列说法正确的是( )

下列说法正确的是( )
| A. | 图3中M表示的是乙的溶解度曲线 | |
| B. | 图2中甲溶液一定饱和,乙溶液不一定饱和 | |
| C. | 图2乙溶液一定比甲溶液浓 | |
| D. | 当W=50g时,甲、乙溶液溶质质量分数一定相等 |

