题目内容
将一定量的碳酸钠溶液与氯化钡溶液混合后,过滤反应的混合物.某研究小组的同学们欲探究滤液中溶质的组成.请你一同参与探究并回答有关问题:
【查阅资料】碳酸钠溶液显碱性;氯化钠、氯化钡溶液显中性.
请你写出碳酸钠溶液与氯化钡溶液反应的化学方程式 .
【提出猜想】
猜想1:滤液中溶质是NaCl;
猜想2:滤液中溶质是NaCl和 (填化学式)的混合物;
猜想3:滤液中溶质是NaCl和Na2CO3的混合物.
【实验探究】
(1)取少量滤液于试管中,滴加2~3滴无色酚酞试液,振荡,无明显现象.同学们认为猜想 不成立.
(2)另取少量滤液于另一支试管中,滴加碳酸钠溶液,若有 (填实验现象)证明猜想2成立.
【问题讨论】
(1)甲同学认为要证明猜想2成立也可以改用硫酸钠溶液.你认为甲同学 (填“能”或“不能”)达到实验目的.
(2)乙同学认为要证明猜想2成立也可以改用硝酸银溶液.你认为乙同学 (填“能”或“不能”)达到实验目的.
| 实验探究物质的组成成分以及含量;盐的化学性质;书写化学方程式、文字表达式、电离方程式. | |
| 专题: | 科学探究. |
| 分析: | 【查阅资料】从碳酸钠溶液与氯化钡溶液反应生成碳酸钡沉淀和氯化钠去分析解答; 【提出猜想】碳酸钠溶液与氯化钡溶液反应生成碳酸钡沉淀和氯化钠,在反应过程中,如果二者恰好完全反应,则滤液中的溶质只有NaCl;若Na2CO3有剩余,则溶液中的溶质除了NaCl还有Na2CO3;若BaCl2有剩余,则溶液中的溶质除了NaCl还有BaCl2去分析解答; 【实验探究】 (1)由【查阅资料】可知:碳酸钠溶液显碱性;氯化钠、氯化钡溶液显中性.酚酞是一种酸碱指示剂,遇碱变红,遇酸不变色;由于“取少量滤液于试管中,滴加2~3滴无色酚酞试液,振荡,无明显现象”说明滤液里面没有碱性的物质去分析解答;. (2)由于结论是猜想2成立,也就是证明滤液中溶质有:NaCl还有BaCl2,加入Na2CO3溶液后,碳酸钠溶液与氯化钡溶液反应生成碳酸钡沉淀和氯化钠,可观察到有白色沉淀(BaCO3)生成去分析解答; 【问题讨论】(1)证明滤液中溶质有:NaCl还有BaCl2,加入Na2SO4溶液后,硫酸钠溶液与氯化钡溶液反应生成硫酸钡沉淀和氯化钠,可观察到有白色沉淀(BaSO4)生成去分析解答; (2)证明滤液中溶质有:NaCl还有BaCl2,加入AgNO3溶液后,NaCl和BaCl2都能和AgNO3反应生成沉淀去分析解答. |
| 解答: | 解:【查阅资料】碳酸钠溶液与氯化钡溶液反应生成碳酸钡沉淀和氯化钠;其化学方程式为:Na2CO3+BaCl2═BaCO3↓+2NaCl;故答案为:Na2CO3+BaCl2═BaCO3↓+2NaCl; 【提出猜想】碳酸钠溶液与氯化钡溶液反应生成碳酸钡沉淀和氯化钠,在反应过程中,如果二者恰好完全反应,则滤液中的溶质只有NaCl;若Na2CO3有剩余,则溶液中的溶质除了NaCl还有Na2CO3;若BaCl2有剩余,则溶液中的溶质除了NaCl还有BaCl2;故答案为:BaCl2; 【实验探究】 (1)由【查阅资料】可知:碳酸钠溶液显碱性;氯化钠、氯化钡溶液显中性.酚酞是一种酸碱指示剂,遇碱变红,遇酸不变色;由于“取少量滤液于试管中,滴加2~3滴无色酚酞试液,振荡,无明显现象”说明滤液里面没有碱性的物质,由题意可知:溶液中没有显碱性的碳酸钠;故答案为:3. (2)由于结论是猜想2成立,也就是证明滤液中溶质有:NaCl还有BaCl2,加入Na2CO3溶液后,碳酸钠溶液与氯化钡溶液反应生成碳酸钡沉淀和氯化钠,反应的化学方程式为:Na2CO3+BaCl2═BaCO3↓+2NaCl;可观察到有白色沉淀(BaCO3)生成;故答案为:沉淀; 【问题讨论】(1)证明滤液中溶质有:NaCl还有BaCl2,加入Na2SO4溶液后,硫酸钠溶液与氯化钡溶液反应生成硫酸钡沉淀和氯化钠,反应的化学方程式为:Na2SO4+BaCl2═BaSO4↓+2NaCl;可观察到有白色沉淀(BaSO4)生成;故答案为:能; (2)证明滤液中溶质有:NaCl还有BaCl2,加入AgNO3溶液后,NaCl和BaCl2都能和AgNO3反应生成沉淀.NaCl和AgNO3反应生成氯化银和硝酸钠,其反应的化学方程式为:NaCl+AgNO3═AgCl↓+NaNO3;BaCl2和AgNO3反应生成氯化银和硝酸钡,其反应的化学方程式为:BaCl2+2AgNO3═2AgCl↓+Ba(NO3)2;无法证明溶液中含有BaCl2;故答案为:不能. |
| 点评: | 考虑化学反应要后剩余的物质时,不但要考虑生成物,还要反应物是否有剩余. |

美国普度大学研发出一种制备氢气的新工艺,流程如下图所示.下列说法错误的是( )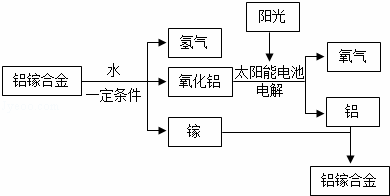
|
| A. | 铝镓合金可以循环使用 |
|
| B. | 太阳能的利用可以部分解决能源危机问题 |
|
| C. | 流程中的氧化铝、水和氧气都属于氧化物 |
|
| D. | 铝镓合金与水反应的化学方程式为:2Al+3H2O |
|
|
|
|
如图为某医用葡萄糖注射液标签的一部分,据此下列说法不正确的是( )

|
| A. | 该葡萄糖注射液中溶质的质量分数为5% |
|
| B. | 葡萄糖的相对分子质量为180 |
|
| C. | 葡萄糖中碳元素、氢元素和氧元素的质量比为1:2:1 |
|
| D. | 在人体组织里,葡萄糖在酶的作用下经缓慢氧化转变成二氧化碳 |
“归纳”“总结”是学习化学常用的方法,下列说法错误的是( )
|
| A. | 通常物质燃烧的条件是:物质具有可燃性、跟氧气接触、温度达到可燃物的着火点,当这三个条件同时具备时燃烧才能发生 |
|
| B. | 复分解反应的条件是:生成物有水、气体、沉淀三个条件至少满足一个.复分解反应才能发生. |
|
| C. | 原子能是有质子、中子、电子三种微粒构成的 |
|
| D. | 不同的物质构成它的基本微粒可能不同,分子、原子、离子都能构成物质 |
下列变化不能一步实现的是( )
|
| A. | KNO3→HCl | B. | Al→Al2O3 | C. | MgCl2→Mg | D. | BaCl2→BaSO4 |
 (1)汽车在行驶过程中的能量转化是__________________________;
(1)汽车在行驶过程中的能量转化是__________________________; Al2O3+3H2
Al2O3+3H2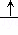
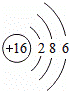 表示 的原子结构示意图;
表示 的原子结构示意图;