题目内容
8.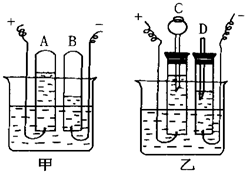 如图,甲、乙两图都是电解水的简易装置,试回答下列问题:
如图,甲、乙两图都是电解水的简易装置,试回答下列问题:(1)装置甲比装置乙有一个明显的优点,这个优点是装置简单,便于操作.
(2)装置乙比装置甲有一个明显的优点,这个优点是便于检验生成物.
(3)在水中加入少量硫酸或氢氧化钠的目的是什么?增强水的导电性.
(4)这一变化的文字表达式是水$\stackrel{通电}{→}$氢气+氧气;,此反应所属的基本类型是分解反应,电解水的实验证明,水是由氢元素和氧元素组成的.
(5)开始电解后,A管收集到氧气,B管收集到氢气.正负极产生的气体体积比为1:2.若已知该条件下氧气的密度为1.429g•L-1,氢气的密度为0.0899g•L-1,则氢气与氧气的质量比为1:8.
(6)在D管处,将使用燃烧着的木条还是带火星的木条进行检验?燃着的木条.
(7)图中显示表明,实验是未开始还是已进行了一段时间?已进行了一段时间.
分析 通过对比可以判断装置的优劣;
通过观察实验现象可以判断实验进行的情况;
可以用燃烧的木条检验生成的氢气,用带火星的木条检验生成的氧气.
解答 解:(1)装置甲比装置乙有一个明显的优点,这个优点是装置简单,便于操作.
故填:装置简单,便于操作.
(2)装置乙比装置甲有一个明显的优点,这个优点是便于检验生成物.
故填:便于检验生成物.
(3)在水中加入少量硫酸或氢氧化钠的目的是增强水的导电性;故填:增强水的导电性.
(4)电解水的文字表达式:水$\stackrel{通电}{→}$氢气+氧气;此反应属于分解反应;电解水的实验证明,水是由氢元素和氧元素组成;答案:水$\stackrel{通电}{→}$氢气+氧气;分解;氢元素和氧元素;
(5)开始电解后,A管收集到气体体积较少,是氧气,B管收集到气体体积较多,是氢气;正极产生的气体是氧气,负极产生的气体是氢气,它们体积比为1:2;则氢气与氧气的质量比为:0.0899g•L-1×2:1.429g•L-1×1=1:8;
故填:氧气;氢气;1:2;1:8.
(6)D试管中收集的是氢气,可以用燃烧的木条检验.
故填:燃着的木条.
(7)试管中聚集了一定量的气体,说明实验已进行了一段时间.
故填:已进行了一段时间.
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,有助于提高观察实验、进行实验的能力.所以,对化学实验不仅要认真观察,还应掌握设计实验、观察实验现象的方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.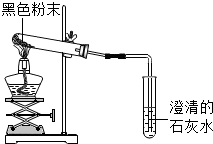 化学小组同学帮助老师整理实验室时,发现一包黑色粉末,老师告诉他们这包粉末是炭粉、铁粉、氧化铜中的两种,为了探究这包黑色粉末的成分,小组同学进行了如下实验:
化学小组同学帮助老师整理实验室时,发现一包黑色粉末,老师告诉他们这包粉末是炭粉、铁粉、氧化铜中的两种,为了探究这包黑色粉末的成分,小组同学进行了如下实验:
【查阅资料】金属氧化物能与酸溶液反应生成可溶性的盐和水.
【提出猜想】猜想一:可能是炭粉和铁粉;猜想二:可能是铁粉和氧化铜
猜想三:可能是炭粉和氧化铜.
【实验验证】
实验一:
实验二:为了验证猜想三成立,小组同学设计了如图实验.
(1)实验中观察到的现象是黑色粉末变红色,澄清石灰水变浑浊,写出两种黑色粉末发生反应的化学方程式2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(2)小红同学认为该装置设计存在问题,你认为该装置缺陷后是没有尾气处理,若产生的气体中含有一氧化碳会污染空气.
 化学小组同学帮助老师整理实验室时,发现一包黑色粉末,老师告诉他们这包粉末是炭粉、铁粉、氧化铜中的两种,为了探究这包黑色粉末的成分,小组同学进行了如下实验:
化学小组同学帮助老师整理实验室时,发现一包黑色粉末,老师告诉他们这包粉末是炭粉、铁粉、氧化铜中的两种,为了探究这包黑色粉末的成分,小组同学进行了如下实验:【查阅资料】金属氧化物能与酸溶液反应生成可溶性的盐和水.
【提出猜想】猜想一:可能是炭粉和铁粉;猜想二:可能是铁粉和氧化铜
猜想三:可能是炭粉和氧化铜.
【实验验证】
实验一:
| 实验操作 | 实验现象 | 实验结论 |
| 取黑色粉末少许,加入过量的 稀盐酸 | 黑色粉末部分溶解,溶液由无色逐渐变为蓝色, | 猜想一和猜想二错误 |
(1)实验中观察到的现象是黑色粉末变红色,澄清石灰水变浑浊,写出两种黑色粉末发生反应的化学方程式2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(2)小红同学认为该装置设计存在问题,你认为该装置缺陷后是没有尾气处理,若产生的气体中含有一氧化碳会污染空气.
19.用Y形管可进行多种实验.
(1)实验一:用酒精喷灯加热左边管内固体,观察到黑色固体变红色;澄清石灰水变浑浊,该Y形管内发生反应的化学方程式为C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O.
(2)实验二:实验过程中可观察到的现象是上面为蓝色粉末变白,下面为白色粉末变蓝,其中发生分解反应的化学方程式为CuSO4•5H2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+5H2O;
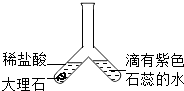
(3)实验三:实验开始1分钟后,右边管内液体变红,该实验所体现的二氧化碳的性质是(用化学方程式表示)CO2+H2O=H2CO3.
| 实验一 | 实验二 | 实验三 |
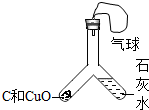 | 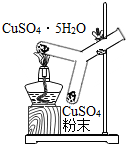 |  |
(2)实验二:实验过程中可观察到的现象是上面为蓝色粉末变白,下面为白色粉末变蓝,其中发生分解反应的化学方程式为CuSO4•5H2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+5H2O;
(3)实验三:实验开始1分钟后,右边管内液体变红,该实验所体现的二氧化碳的性质是(用化学方程式表示)CO2+H2O=H2CO3.
16.下列有关化学观念的叙述,错误的是( )
| A. | 几千万年前地球上一条恐龙体内的某个原子可能在你的身体里 | |
| B. | 为验证空气中含有少量二氧化碳,将大针筒内的空气一次性压入新制的澄清石灰水中,发现石灰水没有变化,为保证实验成功,应继续进行实验 | |
| C. | 用刀切西瓜的过程中,个别原子被分成更小的微粒 | |
| D. | 化学不仅研究物质的性质、组成、结构和变化,还研究变化过程中伴随的能量变化 |
4.下列物质中,既有可燃性,又有还原性的固体单质是( )
| A. | 氢气 | B. | 二氧化碳 | C. | 木炭 | D. | 一氧化碳 |
11.“低碳生活”有望成为新的时尚流行全球,“低碳生活”是指工作生活中所耗能量要减少,从而碱低碳特别是二氧化碳的排气阀,下列不属于“低碳生活”方式的是( )
| A. | 购物自带环保布袋,不用塑料袋 | |
| B. | 将普通灯改为节能灯,使用太阳能热水器 | |
| C. | 夏季在使用空调时,尽量将温度调低 | |
| D. | 多用电邮、QQ等即时通讯工具,少用传真打印机 |
8.同学们在研究二氧化碳实验室制取时,比较了以下四个实验:
(1)实验A中现象是发出白光,放出热量.实验结束后,燃烧的木炭往往用水浇灭,灭火的一个原因是降温至着火点以下.
(2)在实验室,我们不选择实验A、B制取二氧化碳的原因分别是气体不纯、不易收集、反应速率太快、不易收集.实验室制备气体时应考虑:①原料廉价、易得,②反应速率适中.
经过研究,同学们确定了实验室制取二氧化碳的原理,有关化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
| 实验 | A | B | C | D |
| 制取收集 | 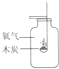 | 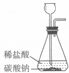 |  | 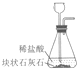 |
(2)在实验室,我们不选择实验A、B制取二氧化碳的原因分别是气体不纯、不易收集、反应速率太快、不易收集.实验室制备气体时应考虑:①原料廉价、易得,②反应速率适中.
经过研究,同学们确定了实验室制取二氧化碳的原理,有关化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
 A、B、C、D都是初中化学中的常见物质,具有如图所示的转化关系(反应条件、有些反应物和生成物已略去).
A、B、C、D都是初中化学中的常见物质,具有如图所示的转化关系(反应条件、有些反应物和生成物已略去).