题目内容
氧化铁的化学式为Fe2O3,试计算:
(1)氧化铁中铁元素的质量分数为
(2)
(1)氧化铁中铁元素的质量分数为
70%
70%
.(2)
25
25
吨含氧化铁80%的铁矿石中含铁14吨.分析:(1)根据化合物中元素的质量分数=
×100%,进行分析解答.
(2)根据题意,设需要铁矿石的质量为x,由氧化铁的质量分数,化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
| 相对原子质量×原子个数 |
| 相对分子质量 |
(2)根据题意,设需要铁矿石的质量为x,由氧化铁的质量分数,化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:(1)氧化铁中铁元素的质量分数为
×100%=70%.
(2)设需要铁矿石的质量为x,
x×80%×70%=14t,x=25t.
故答案为:(1)70%;(2)25.
| 56×2 |
| 56×2+16×3 |
(2)设需要铁矿石的质量为x,
x×80%×70%=14t,x=25t.
故答案为:(1)70%;(2)25.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
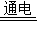 O2↑+2H2↑
O2↑+2H2↑