题目内容
9. 如图是实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算:
如图是实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算:(1)取10.6g碳酸钠与100g该稀硫酸恰好完全反应,求生成气体的质量:
(2)计算上述反应后所得溶液的溶质质量分数.(计算结果保留一位小数)
分析 碳酸钠与稀硫酸反应生成硫酸钠、水和二氧化碳,由参加反应的碳酸钠的质量,由反应的化学方程式列式计算出生成二氧化碳气体的质量、生成硫酸钠的质量,进而计算出反应后所得溶液的溶质质量分数即可.
解答 解:设生成二氧化碳气体的质量为x,生成硫酸钠的质量为y,
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 142 44
10.6g y x
(1)$\frac{106}{44}=\frac{10.6g}{x}$ x=4.4g
(2)$\frac{106}{142}=\frac{10.6g}{y}$ y=14.2g
反应后所得溶液的溶质质量分数为$\frac{14.2g}{10.6g+100g-4.4g}$×100%≈13.4%.
答:(1)生成气体的质量为4.4g;(2)反应后所得溶液的溶质质量分数为13.4%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
18.某实验小组的同学,在6.25克石灰石样品中加入一定溶质质量分数的稀盐酸,每次加入10克,测得数据如下:
试计算:
(1)该石灰石样品中碳酸钙的质量为3g
(2)所用稀盐酸的溶质质量分数.
| 操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| 剩余固体质量 | 5.25g | 4.25g | 3.25g | 3.25g |
(1)该石灰石样品中碳酸钙的质量为3g
(2)所用稀盐酸的溶质质量分数.
14.烧杯中有一定质量的MgO和MgCO3的混合物,向其中加入100g稀盐酸,恰好完全反应.一定温度下,得到102g不饱和溶液.下列数据中,与该溶液的溶质质量分数最接近的是( )
| A. | 2.4% | B. | 3.1% | C. | 2.0% | D. | 4.7% |
1.某化学反应的微观示意图如图所示,有关该化学反应的说法正确的是( )
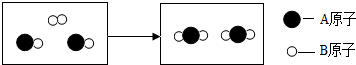

| A. | 反应前后分子个数没变 | B. | 反应前后元素化合价没变 | ||
| C. | 既不是化合反应也不是分解反应 | D. | 化学方程式可表示为:2AB+B2═2AB2 |
19.如表是部分物质的溶解性表(室温),利用表中提供的信息回答下列问题:
(1)NaOH和BaCl2两种物质混合后不能(填“能”或“不能”)发生反应,理由是交换成分没有沉淀、气体或水生成,不符合复分解反应发生的条件.
(2)利用表中阴离子和阳离子构成的物质,写出一个有BaSO4生成的化学方程式BaCl2+Na2SO4═BaSO4↓+2NaCl(合理即可).
| 阴离子 阳离子 | OH- | Cl- | SO42- |
| Na+ | 溶 | 溶 | 溶 |
| Fe2+ | 不 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 |
(2)利用表中阴离子和阳离子构成的物质,写出一个有BaSO4生成的化学方程式BaCl2+Na2SO4═BaSO4↓+2NaCl(合理即可).
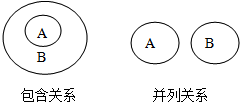 (1)物质分类概念存在如图所示的关系,单质与化合物属于并列关系(填“包含”或“并列”),化合物与氧化物属于包含关系(同上);
(1)物质分类概念存在如图所示的关系,单质与化合物属于并列关系(填“包含”或“并列”),化合物与氧化物属于包含关系(同上);