题目内容
7.为了证明氢氧化钠溶液和稀盐酸发生反应,兴趣小组的同学进行了实验探究.【实验目的】证明氢氧化钠与盐酸发生了化学反应.
【实验原理】HCl+NaOH═NaCl+H2O(用化学方程式表示).
【仪器药品】如图:

【实验方案】
(1)指示剂变色法.
①取A(填“A”或“B”)中试剂加入到D中,滴加2滴酚酞试液,溶液呈红色.
②用G向①中滴加稀盐酸,直到红色刚好消失,证明氢氧化钠与盐酸发生反应.
(2)有新物质生成.
③向②中继续滴加过量稀盐酸的目的是使氢氧化钠完全反应.
④用F蘸取③中溶液,在酒精灯上灼烧,有白色固体产生.将之溶解于少量水中,温度无明显变化,证明不是氢氧化钠,而是生成了新物质.
(3)pH试纸法.
⑤先用pH试纸测定NaOH溶液的pH,再不断滴加稀盐酸并不断振荡溶液,同时多次测定混合溶液的pH,如果测得的pH逐渐变小至等于7或小于7,则证明氢氧化钠与盐酸发生了反应.
(4)热量变化法.
⑥红红在没有使用温度计的情况下,通过设计如图H所示装置顺利完成了实验,她是根据所察到的现象U形管中左边液面下降判断出NaOH溶液与稀盐酸发生了中和反应.
分析 实验原理】
稀盐酸和氢氧化钠反应生成氯化钠和水;
【实验方案】
(1)氢氧化钠能和玻璃中的二氧化硅反应,因此盛放氢氧化钠溶液的试剂瓶瓶塞应该用橡胶塞,氢氧化钠溶液显碱性,能使酚酞试液变红色;
(2)加入足量稀盐酸能使氢氧化钠完全反应;
氢氧化钠溶于水放热;
(3)显碱性溶液pH大于7,显中性溶液pH等于7,显酸性溶液pH小于7;
(4)稀盐酸和氢氧化钠反应放热.
解答 解:实验原理】
稀盐酸和氢氧化钠反应生成氯化钠和水,反应的化学方程式为:HCl+NaOH═NaCl+H2O.
故填:HCl+NaOH═NaCl+H2O.
【实验方案】
(1)①氢氧化钠溶液应该盛放在A试剂瓶中,因此应该取A中试剂加入到D中,滴加2滴酚酞试液,溶液呈红色.
故填:A.
②应该用胶头滴管G向①中滴加稀盐酸,直到红色刚好消失,证明氢氧化钠与盐酸发生反应.
故填:G.
(2)③向②中继续滴加过量稀盐酸的目的是使氢氧化钠完全反应.
故填:使氢氧化钠完全反应.
④用F蘸取③中溶液,在酒精灯上灼烧,有白色固体产生.将之溶解于少量水中,温度无明显变化,证明不是氢氧化钠,而是生成了新物质.
故填:温度无明显变化.
(3)⑤先用pH试纸测定NaOH溶液的pH,再不断滴加稀盐酸并不断振荡溶液,同时多次测定混合溶液的pH,如果测得的pH逐渐变小至等于7或小于7,则证明氢氧化钠与盐酸发生了反应.
故填:如果测得的pH逐渐变小至等于7或小于7.
(4)⑥红红在没有使用温度计的情况下,通过设计如图H所示装置顺利完成了实验,她是根据U形管中左边液面下降,判断出了NaOH溶液与稀盐酸发生了中和反应.
故填:U形管中左边液面下降.
点评 本题阅读量较大,考查了中和反应的概念及其应用,此类问题往往起点高但落点较低,在解题时首先要搞清需要解答的问题,然后应用所掌握的知识逐一分析解答即可.

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案| A. | 将细铁丝放入氧气中,火星四射,生成一种黑色固体 | |
| B. | CO在空气中燃烧,发出淡蓝色火焰,放出热量 | |
| C. | 向盛有铝片的试管中加入稀盐酸,溶液由无色变成浅绿色 | |
| D. | 将红色的铜丝在酒精灯火焰上加热,会变成黑色 |
| A. | 铝原子的核外电子数 | B. | 铝原子最外层电子数 | ||
| C. | 铝元素的相对原子质量 | D. | 铝元素的核电荷数 |
①SO2 ②Mg2+ ③CO2 ④$\stackrel{+2}{Cu}$SO4 ⑤O2- ⑥H2O2 ⑦2O.
| A. | 表示分子个数的是⑦ | |
| B. | 表示离子所带电荷数的是②⑤ | |
| C. | 表示化合价数值的是④ | |
| D. | 表示一个分子中含有某种原子个数的是①③⑥ |
| 温度/℃ | 0 | 20 | 40 | 60 |
| 溶解度/g | 27.6 | 34.0 | 40.0 | 45.5 |
| A. | KCl饱和溶液中不能再溶解其他物质 | |
| B. | 20℃时,100 g KCl饱和溶液中含KCl34.0 g | |
| C. | 40℃时,KCl饱和溶液的质量分数为40.0% | |
| D. | 60℃的KCl饱和溶液降温至20℃,有晶体析出 |
| A. | 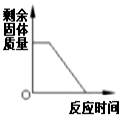 加热一定质量的高锰酸钾固体 | |
| B. | 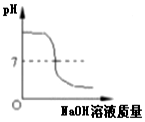 一定量的稀硫酸中滴加氢氧化钠溶液至过量 | |
| C. | 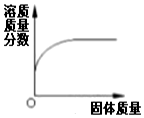 一定温度下,向饱和硝酸钾溶液中不断加入硝酸钾固体,充分搅拌 | |
| D. | 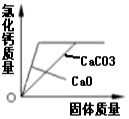 分别向同质量、同质量分数的稀盐酸中不断加入碳酸钙和氧化钙固体 |


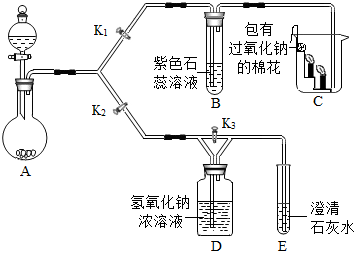 某兴趣小组的同学利用下图装置研究二氧化碳的性质.(仪器的固定装置已经省略)
某兴趣小组的同学利用下图装置研究二氧化碳的性质.(仪器的固定装置已经省略)