题目内容
10.(1)硫酸铜晶体的化学式为CuSO4•5H2O,它俗称蓝矾或胆矾,它的颜色为蓝色,它属于的物质类别是纯净物(填“纯净物”或“混合物”).(2)0.25g胆矾的物质的量是0.001mol,其中含结晶水0.005mol.
(3)计算32g的无水硫酸铜能与多少mol的水发生反应.
分析 (1)根据物质的名称、俗称、颜色以及类别来分析;
(2)根据物质的量的计算方法来分析;
(3)根据化学方程式来分析解答.
解答 解:(1)硫酸铜晶体的化学式为CuSO4•5H2O,是一种蓝色固体,俗称蓝矾或胆矾,是纯净物;故填:CuSO4•5H2O;蓝矾;胆矾;蓝色;纯净物;
(2)0.25g胆矾的物质的量为:0.25g÷250g/mol=0.001mol,由胆矾的化学式可知,其中含结晶水的物质的量为:5×0.001mol=0.005mol;故填:0.001mol;0.005;
(3)解:设与32g无水硫酸铜反应需要水的质量为x,则
CuSO4+5H2O=CuSO4•5H2O
160 90
32g x
$\frac{160}{90}=\frac{32g}{x}$
x=18g
水的物质的量为:18g÷18g/mol=1mol
答:32g的无水硫酸铜能与1mol的水发生反应.
故填:1.
点评 本题考查了物质的名称、俗称及其物理性质,还考查了物质的量的计算,难度不大.

练习册系列答案
相关题目
20.市场上卖出一些加钙牛奶、加铁酱油、加碘的食盐,这里面的“钙、铁、碘”指的是( )
| A. | 分子 | B. | 原子 | C. | 单质 | D. | 元素 |
18.下列知识整理的内容均正确的一组是( )
| A.物质的分类 | B.物质的检验 |
| 乙醇、甲烷和碳酸都是有机物 冰水、雨水和蒸馏水都是混合物 消石灰、纯碱和烧碱都是碱 | 用肥皂水来检验硬水和软水 用灼烧的方法能区别棉花和羊毛 用水能区分熟石灰和氢氧化钠 |
| C.化学与生活、生产 | D.“低碳经济”的措施 |
| 用甲醛溶液浸泡海产品保鲜 硫酸铵不能与草木灰(碱性物质)混合施用 用稀盐酸洗去铁制品表面的铁锈 | 减少煤、石油和沼气等化石燃料的使用 鼓励乘坐公交车出行,倡导低碳生活 开发利用太阳能、风能等新能源 |
| A. | A | B. | B | C. | C | D. | D |
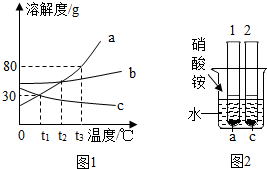 图1所示是a、b、c三种固体物质在水中溶解度曲线,根据如图回答:
图1所示是a、b、c三种固体物质在水中溶解度曲线,根据如图回答:
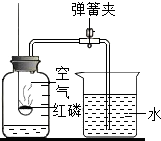 根据下图回答问题:
根据下图回答问题: