题目内容
某化学兴趣小组进行溶液的配制实验。
配制150 g质量分数为10 % 的氢氧化钠溶液。
(1)计算:需要氢氧化钠固体的质量为________g;水的体积为________mL(水的密度近似看作1 g/cm3)。
(2)称量:调节托盘天平平衡后,将 放在托盘天平的左盘,称量其质量。 然后再在右盘添加 。最后添加氢氧化钠固体,直至天平平衡。
(3)溶解:用量 筒量取所需的水,倒入装有氢氧化钠固体的烧杯里,用玻璃棒 ,使其溶解,并冷却至室温。
筒量取所需的水,倒入装有氢氧化钠固体的烧杯里,用玻璃棒 ,使其溶解,并冷却至室温。
(4)存储:把配制好的溶液装入试剂瓶,塞好橡皮塞并 ,放到指定的地方。
(1)15 135 (2)烧杯 砝码 (3)搅拌 (4)贴上标签
解析:(1)配制150 g 质量分数为10% 的氢氧化钠溶液需要氢氧化钠固体的质量为150 g×10%=15 g;需要水的质量为150 g×(1-10%)=135 g。又知水的密度,可求得所需水的体积: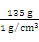 =135 cm3=135 mL。(2)用托盘天平称量物品时应“左物右码”,即左盘放所称量物品,右盘放砝码。(3)溶解过程中,玻璃棒的作用是搅拌,加快溶解速率。
=135 cm3=135 mL。(2)用托盘天平称量物品时应“左物右码”,即左盘放所称量物品,右盘放砝码。(3)溶解过程中,玻璃棒的作用是搅拌,加快溶解速率。
(4)标签上要写明药品名 称和溶液中溶质的质量分数,方便以后查用。
称和溶液中溶质的质量分数,方便以后查用。

某白色固体可能由氢氧化钡(化学式为Ba(OH)2)、氢氧化钠中的一种或两种组成。为确定该固体物质的成分,某![]() 化学兴趣小组进行下列探究活动,请你认真阅读有关信息,回答相关问题。
化学兴趣小组进行下列探究活动,请你认真阅读有关信息,回答相关问题。
【查阅资料】(1) Ba(OH)2是一种强碱,具有NaOH相似的化学性质。
(2)部分酸、碱、盐的溶解性如下表所示:
|
| OH— | Cl— | SO42— | CO32— |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | | 不溶 | 不溶 |
【提出猜想】猜想I :该固体是NaOH
猜想Ⅱ:该固体是Ba(OH)2
猜想Ⅲ:该固体是Ba(OH)2、NaOH的混合物
【设计实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量 | 有白色沉淀出现 | 表明原样品中一定含有 (填化学式) |
| ②向①中继续滴加硫酸钠溶液,直至沉淀不再增加为止,静置后,用pH试纸检测溶液酸碱性 | 溶液呈强碱性 | 表明原样品中还含有氢氧化钠 |
【问题讨论】
(1)实验步骤①中发生反应的化学方程式为 ![]() 。
。
(2)实验步骤②得出的实验结论 (填“正确”或“不正确”)。
(3)如果在上述实验中用稀硫酸代替硫酸钠溶液,实验步骤和实验现象均相同,你可以判断出猜想 是成立的。
 (2013?许昌一模)某化学兴趣小组进行了如图所示的喷泉实验,将胶头滴管中的水挤入烧瓶,然后打开止水夹,在烧瓶内出现美丽的红色喷泉.
(2013?许昌一模)某化学兴趣小组进行了如图所示的喷泉实验,将胶头滴管中的水挤入烧瓶,然后打开止水夹,在烧瓶内出现美丽的红色喷泉.