题目内容
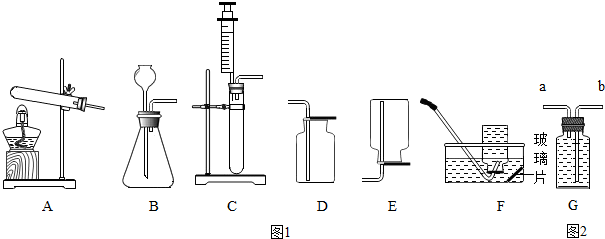
5.现有以下装置、仪器和药品.请根据要求回答问题: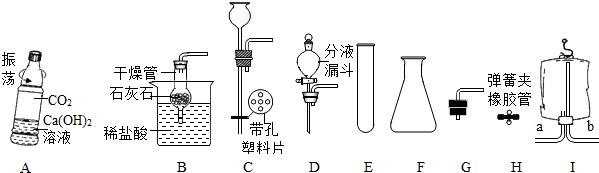
(1)装置B中反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;把H与B组合,操作弹簧夹可以使反应停止或发生,还可从“C至H“中选择仪器C、E、H(填序号)组装一个可随时使反应发生或停止的装置;
(2)若用H2O2和MnO2制取O2,且能获得平稳的气流,应选E(或F)和D组合.
(3)若用I所示医用塑料袋排空气法收集H2,则H2导入端为b(填“a“或“b“).
(4)用A中所示矿泉水瓶可以证明CO2与NaOH溶液确实发生了反应,其现象是矿泉水瓶变瘪,应做的对比实验是取与A同样的装置,倒入同体积的水与CO2混合振荡.
分析 (1)根据石灰石主要成分碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;关闭弹簧夹后酸被压入长颈漏斗,石灰石块状固体就留在C中的带孔塑料板上从而和稀盐酸分离反应停止分析解答;
(2)分液漏斗可以控制双氧水的滴加速度,从而控制产生氧气的速度;
(3)若用图I所示医用塑料袋排空气法收集H2,则H2导入端为b,因为氢气的密度比空气的密度小;
(4)矿泉水瓶变瘪,可以证明CO2与NaOH溶液确实发生了反应;因为二氧化碳能溶于水,能与水反应,因此要做二氧化碳与水反应的对比实验,可取同样的矿泉水瓶,倒入等体积的水振荡,观察矿泉水瓶变瘪的程度进行判断.
解答 解:(1)石灰石主要成分碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;
可以从“C至H”中选择仪器C、E、H,组装一个可随时使反应发生或停止的装置;打开弹簧夹,固体和液体接触产生气体,关闭弹簧夹后试管内气压增大,酸被压入长颈漏斗,石灰石块状固体就留在C中的带孔塑料板上从而和稀盐酸分离反应停止;
(2)分液漏斗可以控制双氧水的滴加速度,从而控制产生氧气的速度,所以若要得到平稳的氧气流,可再选择分液漏斗;
(3)若用图I所示医用塑料袋排空气法收集H2,则H2导入端为b,因为氢气的密度比空气的密度小,所以应从长管进气,将空气挤压到塑料袋底部排出;
(4)二氧化碳和氢氧化钠反应生成碳酸钠和水,则矿泉水瓶内气压减小,瓶子变瘪,因此可通过矿泉水瓶变瘪,证明CO2与NaOH溶液确实发生了反应;
因为二氧化碳能溶于水,能与水反应,因此要做二氧化碳与水反应的对比实验,可取同样的矿泉水瓶,倒入等体积的水振荡,观察矿泉水瓶变瘪的程度进行判断;
故答案为:
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;CEH;
(2)D;
(3)b;
(4)矿泉水瓶变瘪;取与A同样的装置,倒入同体积的水与CO2混合振荡.
点评 本考点主要考查了装置的注意事项、常用仪器的用途、气体的制取装置和收集装置的选择,同时也考查了化学式的书写和实验设计等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案| A. | 硬度 | B. | 导电性 | ||
| C. | 耐腐蚀性 | D. | 与硬币面值相应的价值 |
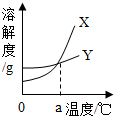 已知氯化钠和硝酸钾的溶解度表与溶解度曲线图如图:
已知氯化钠和硝酸钾的溶解度表与溶解度曲线图如图:| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
| 硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
| A. | X是氯化钠的溶解度曲线 | |
| B. | 溶解度曲线图上的温度a介于10℃~30℃之间 | |
| C. | 60℃时,100g水中加入100g硝酸钾,充分溶解,所得溶液是饱和溶液 | |
| D. | 从硝酸钾和氯化钠(少量)的混合物中分离出硝酸钾常采用蒸发结晶法 |
| A. | 物质的运动状态 | B. | 物质的变化和性质 | ||
| C. | 物质的组成和结构 | D. | 物质的制取和用途 |
| A. | CaO生石灰碱 | B. | Na2CO3纯 碱 碱 | ||
| C. | C2H5OH 酒精 氧化物 | D. | NaHCO3小苏打盐 |