题目内容
13.用电解器电解水时要在水中加少许硫酸钠,以增强其导电.将93.6g质量分数为5%的硫酸钠溶液中通电一段时间后,正极上产生3.2g氧气,计算此时:(1)负极上产生氢气的质量;
(2)溶液中硫酸钠的质量分数.
分析 根据生成的氧气的质量和对应的化学方程式求算生成的氢气的质量,进而求算所得溶液中硫酸钠的质量分数.
解答 解:设生成3.2g氧气时同时生成的氢气的质量为x
2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
4 32
x 3.2g
$\frac{4}{x}=\frac{32}{3.2g}$
x=0.4g
电解后溶液中硫酸钠的质量分数为$\frac{93.6g×5%}{93.6g-3.2g-0.4g}$×100%=5.2%
答:(1)负极上产生氢气的质量为0.4g;
(2)电解后溶液中硫酸钠的质量分数为5.2%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
8. 等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价).下列说法不正确的是( )
等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价).下列说法不正确的是( )
 等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价).下列说法不正确的是( )
等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价).下列说法不正确的是( )| A. | 生成氢气的质量:甲>乙>丙 | B. | 相对原子质量:甲<乙<丙 | ||
| C. | 反应速率:甲>乙>丙 | D. | 消耗硫酸的质量:甲>乙>丙 |
5.下列实验操作正确的是( )
| A. |  称量固体药品 称量固体药品 | B. | 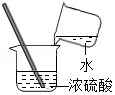 稀释浓硫酸 稀释浓硫酸 | ||
| C. | 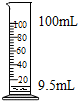 量取9.5mL液体 量取9.5mL液体 | D. |  测定溶液的pH 测定溶液的pH |
3.归纳与反思是学习化学的重要环节,下列各项归纳不完全正确的是( )
| A.化学反应中常见的“三” | B.物质保存方法及解释 |
| 煤、石油、天然气-三大化石燃料 塑料、合成纤维、合成橡胶-三大合成材料 分子、原子、离子-构成物质的三种粒子 | 浓盐酸密封保存-防止挥发 白磷在冷水中保存-隔绝空气 氢氧化钠密封保存-防止潮解、变质 |
| C.化学之最 | D.化学与生活 |
| 熔点最低的金属-汞 地壳中含量最高的金属元素-铁 天然存在的最硬的物质-金刚石 | 衣服上的油污-可用汽油除去 水壶中的水垢-可用食醋浸泡除去 冰箱中的异味-可放活性炭吸附 |
| A. | A | B. | B | C. | C | D. | D |
 图示为中考化学试卷答题卡中用于识别考生信息的条形码(样码).条形码有黏性,其黏性主要来源于胶黏剂丙烯酸.丙烯酸的化学式为C3H4O2.关于丙烯酸,下列说法正确的是C
图示为中考化学试卷答题卡中用于识别考生信息的条形码(样码).条形码有黏性,其黏性主要来源于胶黏剂丙烯酸.丙烯酸的化学式为C3H4O2.关于丙烯酸,下列说法正确的是C