题目内容
14.水煤气是将水蒸气通过灼热的焦炭而生成的气体,主要成分是一氧化碳、氢气及少量的二氧化碳和水蒸气.某课题组同学为验证水煤气的成分,做了以下准备:(一)资料收集:①H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O ②CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2
③无水硫酸铜遇水由白色变为蓝色 ④氢氧化钠溶液能够吸收二氧化碳气体 ⑤浓硫酸有吸水性,可作干燥剂.
(二)设计实验装置
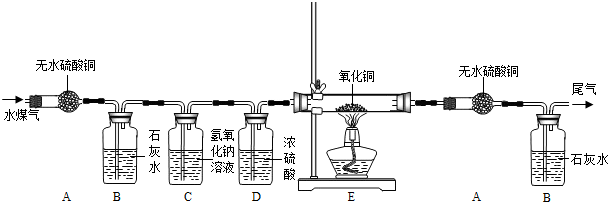
请分析上面信息后回答:
①利用上述装置验证中各成分的依次顺序是H2O、CO2、H2、CO(填气体的化学式);
②装置C的目的是除去水煤气中的二氧化碳,装置D的目的是除去水蒸气,装置E内观察到的现象是黑色固体逐渐变成红色;
③实验中两次用到装置A,其目的分别是第一次使用装置A目的是验证水煤气中水蒸气的存在,第二次使用装置A目的是检验水煤气中是否含有氢气请你设计一种尾气处理方案:将玻璃管改成尖嘴点燃或用气球收集.
分析 ①根据水能使白色硫酸铜变蓝,二氧化碳能使澄清石灰水变浑浊,氢气还原氧化铜能生成水,一氧化碳还原氧化铜生成二氧化碳考虑本题;
②根据氢氧化钠能与二氧化碳反应考虑,浓硫酸有吸水性,氧化铜被还原成铜考虑实验现象;
③根据实验中两次用到装置A,其目的是不同的,第一次用到装置A,其目的是验证水煤气含有二氧化碳气体,第二次用到装置A,其目的是:通过验证生成物中有二氧化碳来证明水煤气中含有一氧化碳.一氧化碳是一种有毒的气体,尾气一般要收集火、点燃进行分析.
解答 解:①水能使白色硫酸铜变蓝,先通过无水硫酸铜是检验是否含有水的;二氧化碳能使澄清石灰水变浑浊,再通过石灰水是检验是否含有二氧化碳的;再通过氢氧化钠是除去原来的二氧化碳气体,通过浓硫酸是除去原来的水蒸气,通过氧化铜是检验是否含有还原性气体,再通过无水硫酸铜,是看是否有水生成,因为氢气还原氧化铜生成铜和水,所以是为了检验是否有氢气的;最后通过澄清石灰水是看有没有二氧化碳生成,由于一氧化碳还原氧化铜生成铜和二氧化碳,所以是为了检验是否含有一氧化碳的;
②氢氧化钠与二氧化碳反应生成碳酸钠和水,所以氢氧化钠的目的是吸收二氧化碳,排除对一氧化碳检验的干扰;浓硫酸有吸水性,所以装置D的目的是:除去水蒸气,氧化铜被还原成铜所以现象是:黑色粉末变为红色;
③前面的装置A是为了检验是否有水生成,后面的装置A是为了检验是否有水生成,从而确定是否有氢气存在,尾气含有一氧化碳,能污染空气,一般要收集火、点燃,所以尾气处理方案:将玻璃管改成尖嘴点燃.
故答案为:①H2O、CO2、H2、CO;
②除去水煤气中的二氧化碳,除去水蒸气,黑色固体逐渐变成红色;
③第一次使用装置A目的是验证水煤气中水蒸气的存在,第二次使用装置A目的是检验水煤气中是否含有氢气,将玻璃管改成尖嘴点燃或用气球收集.
点评 本题难度不是很大,以实验探究的形式考查常见气体氢气、一氧化碳、二氧化碳和水蒸气的性质,熟练掌握常见气体的化学性质并能灵活运用是正确解答本题的关键.

| 元素名称 | 氢 | 碳 | 氧 | 氯 | 锰 | 铁 |
| 元素符号 | H | C | O | Cl | Mn | Fe |
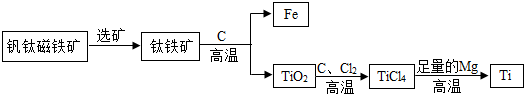
(2)气体单质E与红色固体F在一定条件下反应,得到固体G,反应的化学方程式为3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+2H2O.
(3)将一定量的固体G放入过量M溶液中,能发生反应,观察到的现象是有气泡产生,溶液由无色变成浅绿色.
(4)向(3)所得溶液中加入适量A溶液,溶液变为黄色,且溶质仅有一种,该反应的化学方程式为2FeCl2+2HCl+H2O2=2FeCl3+2H2O.
| A. | 矿泉水 | B. | 空气 | C. | 冰水混合物 | D. | 澄清石灰水 |
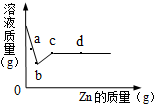 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是( )
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是( )| A. | a点溶液中的溶质有3种 | |
| B. | c点溶液中溶质为Zn(NO3)2、Cu(NO3)2 | |
| C. | 若取a~b段溶液,滴加稀盐酸,有白色沉淀 | |
| D. | 取d点的固体,加入稀盐酸,有气泡产生 |
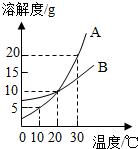 如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )
如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )| A. | 30℃时,将B物质的不饱和溶液转变为饱和溶液,可以采取恒温蒸发溶剂的方法 | |
| B. | A物质的饱和溶液从30℃降温到10℃,变成不饱和溶液 | |
| C. | B物质的饱和溶液从30℃降温到20℃,其溶质质量分数减小 | |
| D. | 30℃时,向100克水中加入25克A物质,充分溶解后所得溶液是饱和溶液 |