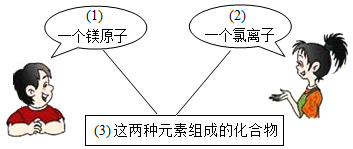
题目内容
19.以下为某实验小组进行的几组实验,根据要求回答问题.(1)为验证稀硫酸化学性质,做如下的三个实验.

实验①最终能观察到的现象是紫色石蕊变蓝色.
实验②能体现出稀硫酸具有的化学性质是酸会与金属氧化物反应.
实验③中发生反应的化学方程式为BaCl2+H2SO4=BaSO4↓+2HCl.
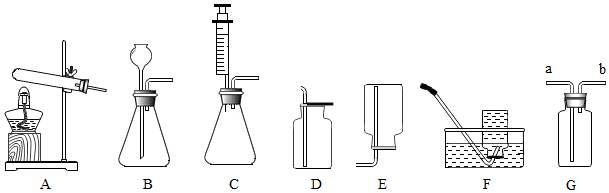
(2)下列所示四个验证实验,不能达到实验目的是B.

分析 (1)①根据酸能使紫色石蕊变红色,碱能使紫色石蕊变蓝色,氢氧化钠会与硫酸反应生成硫酸钠和水进行分析;
②根据氧化铁和硫酸反应生成硫酸铁和水进行分析;
③根据氯化钡和硫酸反应生成硫酸钡沉淀和盐酸进行分析;
(2)A、根据红磷和氧气在点燃的条件下生成五氧化二磷进行分析;
B、根据碳酸钠和盐酸反应生成氯化钠水和二氧化碳,该反应需要在密闭容器中反应进行分析;
C、根据酚酞遇碱变红色进行分析;
D、根据铜不会与稀硫酸反应,铁会与稀硫酸反应,银不会与硝酸汞反应进行分析.
解答 解:(1)①酸能使紫色石蕊变红色,碱能使紫色石蕊变蓝色,氢氧化钠会与硫酸反应生成硫酸钠和水,所以实验①最终能观察到的现象是:紫色石蕊变蓝色;
②氧化铁和硫酸反应生成硫酸铁和水,所以实验②能体现出稀硫酸具有的化学性质是:酸会与金属氧化物反应;
③氯化钡和硫酸反应生成硫酸钡沉淀和盐酸,化学方程式为:BaCl2+H2SO4=BaSO4↓+2HCl;
(2)A、红磷和氧气在点燃的条件下生成五氧化二磷,冷却到室温,打开止水夹,水面上升约五分之一,可以验证空气中氧气的含量,故A正确;
B、碳酸钠和盐酸反应生成氯化钠水和二氧化碳,生成的二氧化碳会逸散到空气中,该反应需要在密闭容器中反应,故B错误;
C、酚酞遇碱变红色,A烧杯中的酚酞变红色,可以验证分子运动,故C正确;
D、铜不会与稀硫酸反应,铁会与稀硫酸反应,银不会与硝酸汞反应,可以验证三种金属的活动性顺序为:铁、铜、汞,故D正确.
故选:B.
故答案为:(1)①紫色石蕊变蓝色;
②酸会与金属氧化物反应;
③BaCl2+H2SO4=BaSO4↓+2HCl;
(2)B.
点评 本题主要考查了酸的化学性质和金属活动性顺序的应用,难度不大,需要在平时的学习中加强记忆即可完成.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目
7.下列图示能正确表示相应化学知识的是( )
| A. |  | |
| B. |  | |
| C. | 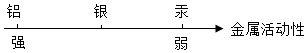 | |
| D. | 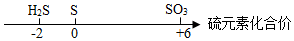 |
4.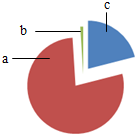 如图为空气成分示意图(按体积计算),其中“c”代表的是( )
如图为空气成分示意图(按体积计算),其中“c”代表的是( )
 如图为空气成分示意图(按体积计算),其中“c”代表的是( )
如图为空气成分示意图(按体积计算),其中“c”代表的是( )| A. | 二氧化碳 | B. | 氮气 | C. | 氧气 | D. | 稀有气体 |
11.下列有关物质的用途与性质,对应关系不正确的是( )
| 选项 | 用途 | 性质 |
| A | 金刚石用于钻探机钻头 | 硬度大 |
| B | 石墨用于制作铅笔芯 | 质软,深灰色 |
| C | N2用作保护气 | 不与任何物质反应 |
| D | CO2用作气体肥料 | 参与光合作用 |
| A. | A | B. | B | C. | C | D. | D |