题目内容
在化学兴趣小组活动中,璇璇同学发现家中有一包标有“生石灰 干燥剂”的小纸袋早已破损,于是将这包生石灰带到学校进行实验.请你与璇璇一起进行探究.
【提出问题】生石灰(CaO)是否变质?变质后的干燥剂中含有那些物质呢?
【提出猜想】璇璇认为变质后的干燥剂的组成有以下几种可能:
①CaO和Ca(OH)2的混合物;②Ca(OH)2;③CaCO3;
④你的猜想是: (写出一种可能)…
【设计并实验】璇璇同学设计并进行了如下实验,请你帮她完成实验报告.
【实验结论】通过以上探究,璇璇得出这包“生石灰干燥剂”已经变质,不能再起干燥作用.
【反思】
(1)生石灰能用作干燥剂是因为 .
(2)Ca(OH)2吸收空气中的CO2而变质,反应的方程式为 .
(3)实验室保存生石灰、熟石灰等化学药品时要注意 保存.
【提出问题】生石灰(CaO)是否变质?变质后的干燥剂中含有那些物质呢?
【提出猜想】璇璇认为变质后的干燥剂的组成有以下几种可能:
①CaO和Ca(OH)2的混合物;②Ca(OH)2;③CaCO3;
④你的猜想是:
【设计并实验】璇璇同学设计并进行了如下实验,请你帮她完成实验报告.
| 实验步骤 | 实验现象 | 结论 |
| ①取少量袋中的固体于烧杯中,加入一定量的水,并用手触摸烧杯壁; | 干燥剂中不含CaO | |
| ②取步骤①烧杯中的少量上层清液于试管中, |
干燥剂中含有Ca(OH)2 | |
| ③另取少量袋中的粉末于试管中,加入稀盐酸. | 产生大量气泡 |
【反思】
(1)生石灰能用作干燥剂是因为
(2)Ca(OH)2吸收空气中的CO2而变质,反应的方程式为
(3)实验室保存生石灰、熟石灰等化学药品时要注意
考点:实验探究物质的组成成分以及含量,证明碳酸盐,生石灰的性质与用途,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【提出猜想】氧化钙和水反应生成氢氧化钙,氢氧化钙易吸收空气中二氧化碳生成碳酸钙,由此解答;
【设计并实验】首先要仔细阅读题中所给的信息,抓到题干中的相关信息.据①的结论:干燥剂中不含CaO,根据知识点生石灰与水变熟石灰放出大量热可知该干燥剂中加入水没有发热现象;氢氧化钙溶液显碱性,所以可向溶液中滴加酚酞试液观察酚酞是否变红判断是否含有氢氧化钙;加足量酸有气泡推断肯定含有碳酸盐那么可以判断出该干燥剂中一定含有碳酸钙,并据反应原理书写方程式;
【反思】(1)氧化钙和水反应生成氢氧化钙,所以可作干燥剂;
(2)据氢氧化钙和二氧化碳反应原理书写方程式;
(3)据(1)(2)可知保存在化学实验室保存氧化钙、氢氧化钙时一定不能漏置在空气中,否则会与空气中的水或二氧化碳发生反应而变质.
【设计并实验】首先要仔细阅读题中所给的信息,抓到题干中的相关信息.据①的结论:干燥剂中不含CaO,根据知识点生石灰与水变熟石灰放出大量热可知该干燥剂中加入水没有发热现象;氢氧化钙溶液显碱性,所以可向溶液中滴加酚酞试液观察酚酞是否变红判断是否含有氢氧化钙;加足量酸有气泡推断肯定含有碳酸盐那么可以判断出该干燥剂中一定含有碳酸钙,并据反应原理书写方程式;
【反思】(1)氧化钙和水反应生成氢氧化钙,所以可作干燥剂;
(2)据氢氧化钙和二氧化碳反应原理书写方程式;
(3)据(1)(2)可知保存在化学实验室保存氧化钙、氢氧化钙时一定不能漏置在空气中,否则会与空气中的水或二氧化碳发生反应而变质.
解答:解:
【提出猜想】氧化钙和水反应生成氢氧化钙,氢氧化钙易吸收空气中二氧化碳生成碳酸钙,由此猜想四是Ca(OH)2和 CaCO3的混合物;
【设计并实验】据①的结论:干燥剂中不含CaO,所以加水应该没有发热现象,或烧杯壁温度没有变化;
氢氧化钙溶液显碱性,所以可向溶液中滴加酚酞试液,据结论干燥剂中含有氢氧化钙,所以酚酞试液变红;
加入足量的盐酸有气泡产生说明该干燥剂中一定含有 CaCO3,碳酸钙能与盐酸反应生成氯化钙、水与二氧化碳,其方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
【反思】(1)氧化钙和水反应生成氢氧化钙,所以可作干燥剂;
(2)氢氧化钙和二氧化碳反应生成碳酸钙和水,化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)由于氧化钙与水反应生成氢氧化钙而变质,氢氧化钙会和空气中的二氧化碳发生反应而变质,所以要密封保存,避免与空气接触;
故答案为:
【提出猜想】Ca(OH)2和 CaCO3的混合物;
【设计并实验】
【反思】(1)氧化钙和水反应生成氢氧化钙;
(2)Ca(OH)2+CO2═CaCO3↓+H2O;
(3)密封保存.
【提出猜想】氧化钙和水反应生成氢氧化钙,氢氧化钙易吸收空气中二氧化碳生成碳酸钙,由此猜想四是Ca(OH)2和 CaCO3的混合物;
【设计并实验】据①的结论:干燥剂中不含CaO,所以加水应该没有发热现象,或烧杯壁温度没有变化;
氢氧化钙溶液显碱性,所以可向溶液中滴加酚酞试液,据结论干燥剂中含有氢氧化钙,所以酚酞试液变红;
加入足量的盐酸有气泡产生说明该干燥剂中一定含有 CaCO3,碳酸钙能与盐酸反应生成氯化钙、水与二氧化碳,其方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
【反思】(1)氧化钙和水反应生成氢氧化钙,所以可作干燥剂;
(2)氢氧化钙和二氧化碳反应生成碳酸钙和水,化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)由于氧化钙与水反应生成氢氧化钙而变质,氢氧化钙会和空气中的二氧化碳发生反应而变质,所以要密封保存,避免与空气接触;
故答案为:
【提出猜想】Ca(OH)2和 CaCO3的混合物;
【设计并实验】
| 实验步骤 | 实验现象 | 结论 |
| ①取少量袋中的固体于烧杯中,加入一定量的水,并用手触摸烧杯壁; | 烧杯壁无发热现象(合理说法均可) | 干燥剂中不含CaO |
| ②取步骤①烧杯中的少量上层清液于试管中,滴加酚酞试液; | 酚酞试液变红 | 干燥剂中含有Ca(OH)2 |
| ③另取少量袋中的粉末于试管中,加入稀盐酸. | 产生大量气泡 | 干燥剂中含有CaCO3,反应的方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑ |
(2)Ca(OH)2+CO2═CaCO3↓+H2O;
(3)密封保存.
点评:本题以生活中常见的食品干燥剂为情境角度出发,考查干燥剂是否变质的问题,以实验探究的形式考查了CO2 Ca(OH )2 CaCO3 三者的性质,特别是考查学生在实验探究中推断分析能力,和平时对含钙化合物的化学性质的积累!

练习册系列答案
相关题目
下列关于实验现象的描述,正确的是( )
| A、红磷在空气中燃烧,产生白色烟雾 |
| B、木炭在氧气里比在空中燃烧剧烈,生成二氧化碳 |
| C、硫在空气中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体 |
| D、纯净的氢气在空气里安静燃烧产生淡蓝色火焰,烧杯壁有小水珠 |
下列化学方程式符合题意且书写正确的是( )
| A、用胃舒乳【Mg(OH)2】治疗胃酸过多:Mg(OH)2+H2SO4═MgSO4+2H2O |
| B、用稀盐酸除铁锈:Fe203+6HCl═2FeCl3+3H2O |
| C、细铁丝在氧气中燃烧:4Fe+3O2═2Fe2O3 |
| D、除去混在硝酸铜溶液中的少量硝酸银:2AgNO3+Cu═Cu(NO3)2+2Ag |
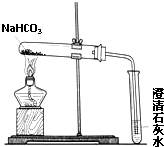 碳酸氢钠是生活中常见的一种盐,在生活中用途广泛.小明同学设计实验对碳酸氢钠的性质进行了探究,请你参与他的探究活动.
碳酸氢钠是生活中常见的一种盐,在生活中用途广泛.小明同学设计实验对碳酸氢钠的性质进行了探究,请你参与他的探究活动.